Автомобіль, маса якого дорівнює 2 т, рушає з місця і їде в гору, для якої h/l = 0,1. На відстані 100 м автомобіль рухався рівно-прискорено і розвинув швидкість 36км/год. Коефіцієнт тертя дорівнює 0,05. Визначити середню потужність двигуна при розгоні (g=10м/с²)
Количество вещества атомов азота в оксидах азота (II) и (IV) равно количеству вещества этих газов, т. к. 1 моль газа содержит 1 моль атомов азота (1 молекула газа содержит 1 атом азота) ; а в оксиде азота (I) количество вещества атомов азота в 2 раза больше, чем количество вещества газа, т. к. 1 моль оксида содержит 2 моль атомов азота (в 1 молеуле оксида - 2 атома азота) .
Т. е. n(N) = 2n(N2O) + n(NO) + n(NO2)
Количество вещества оксида азота (II) дано в условии задачи - 0,125 моль. Найдем количество вещества других оксидов:
n(N2O) = V/Vm = 0,672 л : 22,4 л/моль = 0,03 моль
n(NO2) = m/M = 1,15 г : (14 + 2*16) г/моль = 0,025 моль
Итак, n(N) = 2*0,03 + 0,125 + 0,025 = 0,21 (моль)
Теперь найдем число атомов азота в смеси:
N(N) = n*N(A) = 0,21 моль * 6,02*10^23 моль-1 = 1,2642*10^23 (атомов)
(не пугайтесь: это длинно только с моими объяснениями, а сама запись решения задачи будет значительно короче)
m= 1 кг
Объяснение:
Итак, лужно для начало нагреть лёд при этом мы затратим теплоту Q1 равную:
где c1=2100 Дж/(кг*градус) - удельная теплота нагревания льда, m - масса льда, t= 0 градусов - температура плавления льда, t1= -20 градусов - начальная температура льда.
Далее нужно расплавить этот лёд, затратив теплоту Q2, равную:
где m - масса льда, h=λ=330000Дж/кг - удельная теплота плавления льда.
А далее уже воду получившуюся после плавления льда (и той же массы что и лёд) нужно нагреть до температуры t2=50 градусов:
где с2=4200 Дж/(кг*градус) - удельная теплота нагревания воды.
Всего было затрачена теплота Q=5.82*10^5:
Q=Q1+Q2+Q3=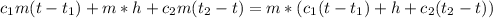
Отсюда масса льда/воды:
Вот и ответ
:)