Питома теплота пароутворення азоту становить 0,2 МДж/кг . Яку кількість теплоти необхідно передати азоту масою 2500г , узятому за температури кипіння , щоб перетворити його на пару ?
Изохорный процесс- термодинамический процесс, который происходит при постоянном объёме. Для осуществления изохорного процесса в газе или жидкости достаточно нагревать или охлаждать вещество в сосуде неизменного объёма. В изохорном процессе (V = const) газ работы не совершает, A = 0. Следовательно,
Q = ΔU = U(T2) – U(T1).
Здесь U(T1) и U(T2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0).
Изобарный процесс- термодинамический процесс, происходящий в системе при постоянных давлении и массе газа.
В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением
A = p(V2 – V1) = pΔV.
+Первый закон термодинамики для изобарного процесса дает:
Q = U(T2) – U(T1) + p(V2 – V1) = ΔU + pΔV.
При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T2 < T1; внутренняя энергия убывает, ΔU < 0.
Изотермический процесс- термодинамический процесс, происходящий в физической системе при постоянной температуре. Для осуществления изотермического процесса систему обычно помещают в термостат (массивное тело, находящееся в тепловом равновесии), теплопроводность которого велика, так что теплообмен с системой происходит достаточно быстро по сравнению со скоростью протекания процесса, и, температура системы в любой момент практически не отличается от температуры термостата. В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0.
Первый закон термодинамики для изотермического процесса выражается соотношением Q = A.
Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам.
Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами. Сосуды с теплонепроницаемыми стенками называются адиабатическими оболочками, а процессы расширения или сжатия газа в таких сосудах называются адиабатическими.
Разделим путь полета тела на разные промежутки.
Пусть до последних четырех секунд тело пролетело S₁ м, за предпоследние две секунды тело пролетело S₂ м, а за последние две секунды S₃ м.
Рассмотрим конкретно участки S₂ и S₃.
Время t₂ = t₃ = 2 с ;
Ускорение g = 10 м/с² ;
Начальные скорости v₀₂ и v₀₃ разные. Найдем v₀₂, то есть скорость падения в момент начала пути S₂.
Мы знаем, что S₃ = 2S₂.
Найдем сумму этих путей, понимая, что сумма этих путей это S₂₃, где
t = 4 с ; g = 10 м/с^2 ; v₀ = v₀₂ ;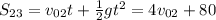
и одновременно подставим все данные значения:
S₂ = 20 + 20 = 40 м
S₃ = 2S₂ = 80 м
Мы знаем, что путь S₁ тело пролетело с ускорением g и набрало скорость от v₀₁ = 5 до v₀₂ = 10 м/с.
По формуле:
S₁ = 3,75 м
Время за первую часть полёта:
t₁ = 0,5 с
Общий путь (высота, с которой сбросили тело):
h = S = S₁ + S₂ + S₃ = 3,75 м + 40 м + 80 м = 123,75 м
Общее время (время падения):
t = t₁ + t₂ + t₃ = 0,5 с + 2 с + 2 с = 4,5 с
1) h = 123,75 м
2) t = 4,5 с
Изохорный процесс- термодинамический процесс, который происходит при постоянном объёме. Для осуществления изохорного процесса в газе или жидкости достаточно нагревать или охлаждать вещество в сосуде неизменного объёма. В изохорном процессе (V = const) газ работы не совершает, A = 0. Следовательно,
Q = ΔU = U(T2) – U(T1).
Здесь U(T1) и U(T2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0).
Изобарный процесс- термодинамический процесс, происходящий в системе при постоянных давлении и массе газа.
В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением
A = p(V2 – V1) = pΔV.
+Первый закон термодинамики для изобарного процесса дает:
Q = U(T2) – U(T1) + p(V2 – V1) = ΔU + pΔV.
При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T2 < T1; внутренняя энергия убывает, ΔU < 0.
Изотермический процесс- термодинамический процесс, происходящий в физической системе при постоянной температуре. Для осуществления изотермического процесса систему обычно помещают в термостат (массивное тело, находящееся в тепловом равновесии), теплопроводность которого велика, так что теплообмен с системой происходит достаточно быстро по сравнению со скоростью протекания процесса, и, температура системы в любой момент практически не отличается от температуры термостата. В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0.
Первый закон термодинамики для изотермического процесса выражается соотношением Q = A.
Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам.
Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами. Сосуды с теплонепроницаемыми стенками называются адиабатическими оболочками, а процессы расширения или сжатия газа в таких сосудах называются адиабатическими.