1.Положительные степени окисления могут проявлять: а) все галогены; б) все галогены, кроме фтора и хлора;
в) все галогены, кроме иода; г) все галогены, кроме фтора.
2.Прямой реакцией галогена с металлом нельзя получить соль, формула которой:
а) Cu F2; б) FeCl2 ; в) CaBr2 ; г) Na I ;
Напишите уравнения реакций трёх остальных веществ.
3.Реакция между какими веществами невозможна:
а) бромной водой и иодидом калия; б) бромной водой и раствором хлорида натрия;
в) хлорной водой и раствором бромида цезия;
г) хлорной водой и раствором иодида калия;
Напишите уравнения реакций, которые возможны.
4.Молекула гормона тироксина содержит 4атома иода, массовая доля которого в веществе
составляет 65,4%. Молярная масса тироксина равна:
а) 777г/моль; б)194г/моль; в) 388г/моль; г)583г/моль.
5.В лаборатории хлор получают окислением конц. соляной кислоты сильным окислителем, например перманганатом калия. Помимо хлора продуктами реакции являются:
а) хлорид калия, оксид марганца(IV), вода;
б) хлорид калия, хлорид марганца (IV), вода;
в) гидроксид калия, хлорид марганца (II), вода;
г) хлорид калия, гидроксид марганца (II), вода.
Попробуйте написать уравнение реакции и уравнять методом эл. баланса.
6.Слёзы, пот, кровь и другие физиологические жидкости имеют солоноватый привкус. Доказать
наличие хлорид-аниона в капле слезы можно с раствора:
а) гидроксида натрия; б)сульфата меди (II); в)нитрата серебра; г) брома в воде.
Напишите ионное уравнение реакции.
7.Соляная кислота может проявлять:
а) только окислительные свойства;
б) только восстановительнве свойства;
в) как окислительные, так и восстановительные свойства;
г) верного ответа среди перечисленных выше нет.
Докажите свой ответ соответствующими уравнениями реакций.
8.Иод в промышленности плучают окислением иодид-ионов, содержащихся в буровых водах,
хлором. Напишите сокращённое ионное уравнение этого процесса. Сумма коэффициентов в уравнении равна:
а) четырём; б) пяти; в)шести; семи;
9.Криолит, имеющий формулу Na3 AlF6, используют:
а) для получения фтора;
б) при производстве алюминия;
в) в качестве сырья для получения натрия;
г) как фторсодержащая добавка к зубной пасте.
10. Дана схема превращений:
Вr ---HBrZn Br Ag Br ---Na Br .
Какое из превращений невозможно осуществить в одну стадию:
А)1; б)2; в)3; г) 4;
8,5 г х г
170 г 143,5 г
1. Найдем теоретически возможную массу осадка:
при взаимодействии 170 г нитрата выпадает 143,5 г хлорида, а
при -- // -- 8,5 г_________________х г, откуда
х=8,5*143,5/170=7,18 г
2. Выход продукта - это отношение практической массы продукта реакции(дана по условию задачи и составляет 7 г) к теоретически возможной :
выход продукта=m практическая(AgCl)/m теоретическая(AgCl)=7/7,18=0,97 или 97%
Вот решение:
Дано:
V(смеси) = 150л
W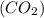 = 15%
= 15%
Найти:
В данной смеси:
V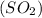 - ?
- ?
V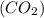 - ?
- ?
Друг, здесь чистая математика:
1) Поскольку объёмная доля последнего составляет 15%, т.е W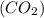 = 15%, найдём сколько литров
= 15%, найдём сколько литров 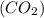 находится в данной смеси:
находится в данной смеси:
Значит, всего 150л-это 100%. Обозначим за x- неизвестный объём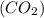 , значит xл- это 15%. Составим пропорцию:
, значит xл- это 15%. Составим пропорцию:
150л-100%
xл-15% => xл=15% * 150л / 100%= 22,5л.;
2) Дальше, мы знаем, что у нас 22,5 л.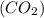 , т.е V
, т.е V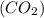 = 22,5л находится в смеси объёмом 150л, а значит объём
= 22,5л находится в смеси объёмом 150л, а значит объём 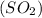 будет равен: 150л-22,5л=127,5л, т.е V
будет равен: 150л-22,5л=127,5л, т.е V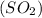 = 127,5л. Всё!
= 127,5л. Всё!
ответ: V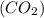 = 22,5л; V
= 22,5л; V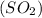 = 127,5л.
= 127,5л.
-------------------------------------------------------------------------------------------------
Есть вопросы? Задавай Тык