1. Сформулируйте Периодический закон, данный Д.И.Менделеевым.
2. Какую характеристику химических элементов взял Д.И.Менделеев за основу их классификации?
3. Какие ряды химических элементов называют периодами?
4. Какие бывают периоды?
5. В чем физический смысл номера периода?( показывает число протонов, число электронов в атоме данного элемента)
6. Какие ряды химических элементов называют группой? Группы делятся на …
7. Какие подгруппы называются главными, побочными?
8. Дайте определение атома.
9. Какие элементарные частицы входят в состав атома? Какой они имеют заряд?
10. Что такое изотопы? Назовите изотопы водорода.
11. Дайте современную формулировку периодического закона.
12. Что лежит в основе периодичности свойств химических элементов с современной точки зрения?
13. В чем физический смысл порядкового номера?
14. Элементы, каких семейств относятся к главным подгруппам?
15. Элементы, каких семейств относятся к побочным подгруппам?
16. Как изменяются свойства химических элементов в группах?
17. В чем физический смысл номера группы? ( показывает число электронов на последнем энергетическом уровне атома находящегося в главной подгруппе элементов)
Ионы это когда атомы отдают или получают один, два атома для того, чтобы приблизится к благородным газам. Эти благородные газы имеют 8 атомов во внешнем пути, эти 8 атомов на внешнем уровне - цель всех атомов. Давай расмотрим на примере Натрия и Хлора.
У натрия и три уровня, во внешнем 1 атом, во втором 8. ЧТобы стать благородным он должен избавится от этого одного атома. У хлора тоже три уровня, однако на внешнем уровне 7 атомов, то есть чтобы стать благородным ему нужен только один атом. При их соединении атом натрия отдаст свой внешний уровень хлору, благодаря чему тот кто отдал станет положительно заряженым, тот кто взял отрицательно.
Ионная связь может быть ТОЛЬКО МЕЖДУ металлами и неметаллами. То есть таковыми могут быть соеденения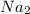 О, KCl
О, KCl
Дано:
m(технического фосфора)=65г.
ω%(примесей)=2%
Vm=22,4л./моль
V(O₂)-?
1. Определим массу примесей в техническом фосфоре:
m(примесей)=ω%(примесей)×m(технического фосфора)÷100%
m(примесей)=2%×65г.÷100%=1,3г.
2. Определим масу чистого фосфора:
m(P)=m(технического фосфора)-m(примесей)
m(P)=65г.-1,3г.=63,7г.
3. Определим молярную массу фосфора:
M(P)=31г./моль
4. Определим количество вещества фосфора в 63,7г.:
n₁(P)=m(P)÷M(P)
n₁(P)=63,7г.÷31г./моль=2моль
5. 4P+5O₂=2P₂O₅
по уравнению реакции:
n(P)=4моль (O₂)=5моль
по условию задачи:
n₁(P)=2моль n₁(O₂)=2,5моль
6. Определим объем кислорода количеством вещества 2,5моль:
V(O₂)= n₁(O₂)xVm
V(O₂)=2,5мольх22,4л./моль=56л.
7. ответ: 56л. кислорода вступит в реакцию с фосфором.