1)слили два раствора серной кислоты: 250г 6% раствора и 150г 20%. определите массовую долю кислоты в полученном растворе. 2)найдите объем водорода(н.у), который полностью прореагирует с кислородом количеством 0,6 моль. 3)определить вид связи соединениях. напишите схемы образования связи; a) hcl б)o2 в)caf
1) Найдем массы чистой (безводной) серной кислоты в растворах:
ω=m(в-ва)÷m(р-ра)×100% ⇒ m(в-ва)=ω×m(р-ра)÷100%
m₁(H₂SO₄)=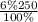 =15 г H₂SO₄
=15 г H₂SO₄
m₂(H₂SO₄)=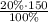 =30 г H₂SO₄
=30 г H₂SO₄
Масса образовавшегося раствора:
m(р-ра)= m₁(р-ра)+m₂(р-ра) = 250+150 = 400 г
Общая масса чистой (безводной) кислоты:
m(H₂SO₄)=m₁(H₂SO₄)+m₂(H₂SO₄)=15+30=45 г
Массовая доля H₂SO₄ в образовавшемся растворе:
ω=m(в-ва)÷m(р-ра)×100% ⇒ ω=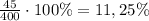
ответ: массовая доля кислоты 11,25%.
2) 2Н₂ + О₂ = 2Н₂О
V(O₂)= 0,6·22,4= 13,44 л
Vm(Н₂)= 22,4 л/моль
Vm(О₂)= 22,4 л/моль
V(Н₂)= х л
V(О₂)= 13,44 л
Расчет по уравнению реакции:
2×22,4 л Н₂ реагирует с 22,4 л О₂
х л Н₂ реагирует с 13,44 л О₂
ответ: водорода потребуется 26,88 л.
3) а) HCl - ковалентная полярная связь
б) O₂ - ковалентная неполярная связь
в) CaF - ионная связь