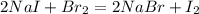1.В предложенном списке укажите утверждение, в котором указана причина
того, что растворы электролитов проводят электрический ток:
1оба утверждения верны
2образование катионов и анионов под действием электрического тока
3образование ионов в растворе
4нет подходящего ответа
2.В предложенном перечне укажите название электролита, при диссоциации которого в качестве катионов образуются только катионы водорода:
1гидроксид магния
2нитрат натрия
3азотистая кислота
4дигидрофосфат кали
3.В предложенном перечне отыщите название электролита, при диссоциации которого в качестве анионов образуются только гидроксид-ионы:
1сероводородная кислота
2фосфат калия
3гидроксид натрия
4гидросульфат натрия
4.В предложенном перечне отыщите название электролита, при диссоциации которого образуются катионы металла (или катион аммония) и анионы кислотного остатка:
1гидроксид кальция
2фосфорная кислота
3угольная кислота
4хлорид натрия
5.В предложенном перечне отыщите верное утверждение:
при диссоциации оснований образуются катионы гидроксогрупп
нет подходящего ответа
при диссоциации оснований образуются гидроксид-ионы
при диссоциации кислот образуются катионы кислотного остатка
6.Выберите ряд, в котором все предложенные вещества диссоциируют по ступеням:
1сульфат аммония, фосфат натрия
2фосфорная кислота, соляная кислота
3сероводородная кислота, сернистая кислота
4азотная кислота, фосфорная кислота
Дано:
m (MgO) = 8 г
W (примесей) = 15% или 0,15
Найти:
m(Mg(NO3)2 = ?
Найдём массовую долю оксида магния: w (MgO) = 1 - 0,15 = 0,85
Найдём чистую массу оксида магния: m(MgO) = 0,85 x 8 = 6,5 г
6,5 г х г
MgO + 2HNO3 = Mg(NO3)2 + H2O
1 моль 1 моль
n(MgO) : n(Mg(NO3)2) = 1:1 => n(MgO) = n(Mg(NO3)2)
n(MgO) = m/M = 6,5 г делим на 40 г/моль = 0,1625 моль, округляем до 0,17 => n (Mg(NO3)2 = 0,17 моль
M(MgO) = 24 + 16 = 40 г/моль
Зная молекулярную массу и количество вещества, можно вычислить массу продукта: m (Mg(NO3)2) = M уможаем на n = (24 + 14х2 +16х6=148) г/моль x 0,17 моль = 25,16 г.
ответ: m (Mg(NO3)2) = 25,16 г.
P(с.о. 0) - 3е = P(с.о. +3)
Br2 (с.о. 0) +1e х 2 = 2Br (с.о. -1)
НОК - 6, следовательно у фосфора коэффициент получаем 2, а у брома - 3. Тройка в продукте реакции уже есть, значит, нужно поставить только двойку перед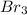 . Затем уравниваем фосфор и бром, и получается:
. Затем уравниваем фосфор и бром, и получается: 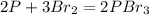 . Восстановителем является фосфор (процесс - окисление), а окислителем - бром (процесс, соответственно, восстановление).
. Восстановителем является фосфор (процесс - окисление), а окислителем - бром (процесс, соответственно, восстановление).
Br2 (с.о. 0) +1e х 2 = 2Br (с.о. -1) - окислитель, восстановление
2I (с.о. -1) - 1e х 2 = I2 (с.о. 0) - восстановитель, окисление
Получается: