У нас известна массовая доля углерода в соединении, давайте попробуем вытянуть из нее
число атомов углерода. Мы знаем, что молекулярная масса равняется сумме атомных масс элементов, для нашего спирта "мистер ИКС" она выглядит вот так: 14n + 18, это уравнение справедливо для всей предельных одноатомных спиртов.
Распишем получение массовой доли углерода:
, упростим выражение:
9.0846n + 11.6748 = 12n - видим, что получилось уравнение с одним неизвестным, причем простое, линенйное. Округлим его.
9n + 12 = 12n, сократим на 3
3n + 4 = 4n
отсюда n= 4 , значит спирт имеет вот такуб формулу:
Запишем уравнение горения:
Рассчитаем количество вещества спирта:
n = m/M = 1,48г/74г/моль = 0,02моль
По уравнению реакции:
n(CO2) = 4n(C4H9OH) = 0,02моль*4 = 0,08моль
Теперь, разберемся со второй реакцией, с едким кали:
CO2 + KOH =
Мы не можем предсказать какие точно будут продукты, тут возможны два варианта, либо карбонат калия, либо гидрокарбонат, зависит от того в избытке дана щелочь или нет.
Рассчитаем количество вещества щелочи.
моль
Я сразу нашел количество вещества, в числителе я умножил плотность на объем и на массовую долю, таким образом нашел массу KOH в растворе, а затем разделил на его молярную массу.
Видим, что n(CO2) = 0,08 моль, а n(KOH) = 0,26 моль, значит, CO2 - в недостатке и образуется карбонат калия, пишем уравнение:
CO2 + 2KOH = K2CO3 + H2O
Рассчитаем массу соли.
По уравнению реакции: n(K2CO3) = n(CO2) = 0,08моль
Рассчитаем массу: m = n*M = 0,08моль*202г/моль = 16,16г
1) С2H6+Сl2=> CH3-CH2-Cl +HCl
CH3-CH2-Cl+ NaOH(спиртовой)= С2H4
С2H4 (Ni.дегидрирование)=> C2H2 +H2
C2H2+HCl=> CH2=CH-Cl
2) 2CH4=> C2H2+ 3H2
C2H2+H2(кат. Ni)=> C2H4
C2H4(Ni,дегидрирование)=С2H2 +H2
3C2H2(тримеризация, кат. активированный уголь)=>C6H6
3)Внутримолекулярная дегидратация, кат. H2SO4, t 180
C2H5OH => C2H4 +H2O
C2H4(дегидрирование, кат Ni)=>C2H2затем снова тримеризация=>C6H6
C6H6 +HNO3=> C6H5NO2
4) CaCO3=>CaO+CO2 CaO+3C=>CaC2+CO
CaC2+2H2O=> Ca(OH)2+C2H2
C2H2+H2=> C2H4
C2H4 +HCl=> CH3-CH2-Cl
Давайте обозначим неизвестный спирт как: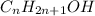
Запишем уравнения протекающих реакций:
У нас известна массовая доля углерода в соединении, давайте попробуем вытянуть из нее
число атомов углерода. Мы знаем, что молекулярная масса равняется сумме атомных масс элементов, для нашего спирта "мистер ИКС" она выглядит вот так: 14n + 18, это уравнение справедливо для всей предельных одноатомных спиртов.
Распишем получение массовой доли углерода:
9.0846n + 11.6748 = 12n - видим, что получилось уравнение с одним неизвестным, причем простое, линенйное. Округлим его.
9n + 12 = 12n, сократим на 3
3n + 4 = 4n
отсюда n= 4 , значит спирт имеет вот такуб формулу:
Запишем уравнение горения:
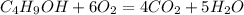
Рассчитаем количество вещества спирта:
n = m/M = 1,48г/74г/моль = 0,02моль
По уравнению реакции:
n(CO2) = 4n(C4H9OH) = 0,02моль*4 = 0,08моль
Теперь, разберемся со второй реакцией, с едким кали:
CO2 + KOH =
Мы не можем предсказать какие точно будут продукты, тут возможны два варианта, либо карбонат калия, либо гидрокарбонат, зависит от того в избытке дана щелочь или нет.
Рассчитаем количество вещества щелочи.
Я сразу нашел количество вещества, в числителе я умножил плотность на объем и на массовую долю, таким образом нашел массу KOH в растворе, а затем разделил на его молярную массу.
Видим, что n(CO2) = 0,08 моль, а n(KOH) = 0,26 моль, значит, CO2 - в недостатке и образуется карбонат калия, пишем уравнение:
CO2 + 2KOH = K2CO3 + H2O
Рассчитаем массу соли.
По уравнению реакции:
n(K2CO3) = n(CO2) = 0,08моль
Рассчитаем массу:
m = n*M = 0,08моль*202г/моль = 16,16г
Изомеры:
CH3 - CH2 - CH2 - CH2 - OH - н - бутиловый спирт(бутанол - 1)
CH3 - CH - CH2 - OH 3 - метилпропанол - 1
|
CH3
CH3 - CH2 - CH - OH 2 - метилпропанол - 1
|
CH3
CH3 - CH2 - CH - CH3 бутанол - 2
|
OH
CH3
|
CH3 - C - CH3 2 метил - пропанол - 2
|
OH
CH3 - O - CH2 - CH2 - CH3 метилпропиловый эфир
СH3 - CH2 - O - CH2 - CH3 диэтиловый эфир
CH3 - CH2 - CH2 - O - CH3 пропилметиловый эфир