1) В пределах одной группы металлические свойства возрастают при увеличении порядкового номера элемента. Это связано с увеличением радиуса атома и более легким отхождением электронов от ядра.
ОТВЕТ: а)
2) Имея только один электрон на внешнем энергетическом уровне, элемент может иметь валентность только 1, соответственно может содержать только одну ОН группу и два атома на кислород в окисде.
ОТВЕТ: в)
3) Как уже было сказано в первом номере, в одной группе радиус атома увеличивается с увеличением его порядкового номера.
ОТВЕТ: г)
4) Щелочные металлы невероятно активны, и всячески стремятся перейти в устойчивую для себя форму иона, с зарядом +1. Поэтому в свободной форме в природе не встречаются и окислительных свойств не проявляют почти совсем, а восстановительных в степени окисления +1 в принципе не могут проявлять, но что правда про них, это то, что их действительно почти все можно спокойно резать ножом и намазывать на хлеб, главное потом не есть)
ОТВЕТ: в)
5) Реакция натрия с водой невероятно экзотермична. Натрий как бешеный носится по поверхности и искрит. В то же время это является реакцией замещения водорода на натрий. Продуктом реакции является щелочь.
ОТВЕТ: в)
6) Основные свойства щелочей тем выше, чем активнее металл, входящий в соединение наиболее активным металлом является литий.
ОТВЕТ: а)
7) С раствором щелочи точно не могут взаимодействовать основные соединения. Могут лишь кислотные и амфотерные. Могут таже растворимые соли, если в результате реакции получается нерастворимвый гидроксид.
ОТВЕТ: б)
8) Соли натрия содержает его ионы. Ионы натрия окрашивают пламя горелки в желтый цвет.
ОТВЕТ: г)
9) Каустическая сода (она же едкий натр) - тривиальное название гидроксида натрия
Угольная и кремниевая кислоты (Н2СО3, H2SiO3) — слабые кислоты.
Кремниевая кислота слабее угольной. В водных растворах угольная кислота вытесняеткремниевую из их солей.
Водородные соединения: СН4; SiH4.
Метан — CH4 — прочное соединение,
силан SiH4- менее прочное соединение.
Схемы строения атомов углерода и кремния, общие и отличительные свойства.
С lS22S22p2;
Si 1S22S22P63S23p2.
Углерод и кремний - это неметаллы, так как на внешнем электронном слое 4 электрона. Но так как кремний имеет больший радиус атома, то для него более характерна отдавать электроны, чем для углерода. Углерод — восстановитель.
1) В пределах одной группы металлические свойства возрастают при увеличении порядкового номера элемента. Это связано с увеличением радиуса атома и более легким отхождением электронов от ядра.
ОТВЕТ: а)
2) Имея только один электрон на внешнем энергетическом уровне, элемент может иметь валентность только 1, соответственно может содержать только одну ОН группу и два атома на кислород в окисде.
ОТВЕТ: в)
3) Как уже было сказано в первом номере, в одной группе радиус атома увеличивается с увеличением его порядкового номера.
ОТВЕТ: г)
4) Щелочные металлы невероятно активны, и всячески стремятся перейти в устойчивую для себя форму иона, с зарядом +1. Поэтому в свободной форме в природе не встречаются и окислительных свойств не проявляют почти совсем, а восстановительных в степени окисления +1 в принципе не могут проявлять, но что правда про них, это то, что их действительно почти все можно спокойно резать ножом и намазывать на хлеб, главное потом не есть)
ОТВЕТ: в)
5) Реакция натрия с водой невероятно экзотермична. Натрий как бешеный носится по поверхности и искрит. В то же время это является реакцией замещения водорода на натрий. Продуктом реакции является щелочь.
ОТВЕТ: в)
6) Основные свойства щелочей тем выше, чем активнее металл, входящий в соединение наиболее активным металлом является литий.
ОТВЕТ: а)
7) С раствором щелочи точно не могут взаимодействовать основные соединения. Могут лишь кислотные и амфотерные. Могут таже растворимые соли, если в результате реакции получается нерастворимвый гидроксид.
ОТВЕТ: б)
8) Соли натрия содержает его ионы. Ионы натрия окрашивают пламя горелки в желтый цвет.
ОТВЕТ: г)
9) Каустическая сода (она же едкий натр) - тривиальное название гидроксида натрия
ОТВЕТ: в)
10) Хлорид соединие вида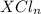 , сульфид
, сульфид 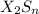 , гидрид
, гидрид 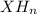 .
.
ОТВЕТ: в)
Угольная и кремниевая кислоты (Н2СО3, H2SiO3) — слабые кислоты.
Кремниевая кислота слабее угольной. В водных растворах угольная кислота вытесняеткремниевую из их солей.
Водородные соединения: СН4; SiH4.
Метан — CH4 — прочное соединение,
силан SiH4- менее прочное соединение.
Схемы строения атомов углерода и кремния, общие и отличительные свойства.
С lS22S22p2;
Si 1S22S22P63S23p2.
Углерод и кремний - это неметаллы, так как на внешнем электронном слое 4 электрона. Но так как кремний имеет больший радиус атома, то для него более характерна отдавать электроны, чем для углерода. Углерод — восстановитель.
1) реагирует с активными металлами: