Домашнее задание №2 «Общие закономерности химических процессов» Вариант 16
Для реакции
Fe3O4(к) +4H2(г) ↔ 3Fe(к) + 4H2O(г)
Пренебрегая температурной зависимостью, вычислите стандартные изменения энтальпии, энтропии, энергии Гиббса.
Сделайте вывод о возможности протекания реакции в прямом направлении при высоких и низких температурах.
Напишите математическое выражение константы химического равновесия, укажите направление смещения равновесия
- при понижении температуры
- понижении давления.
1 рівень
1. а
2. б
3. а,б
4. в
5. б
6. б
2 рівень
1. 2Cu + O2 → 2CuO - оксид міді
2. 4 Al (s) + 3 O2 (g) → 2 Al2O3 - оксид алюмінію
3. 4 P + 5 O2 → 2 P2O5 - оксид фосфору
3 рівень
1.
2 С2Н6 + 7 О2 → 4 СО2 + 6 Н2О
2 РН3 + 4 О2 → Р2О5 + 3 Н2О
4 В +3 O2= 2 В2О3
2. Мr(Аl2О3) = 2Аr(Аl) + ЗАr(O);
Мr(Аl2О3) = 2 • 27 + 3 • 16 = 102;
ω (Al в Al2O3) = N (Al в Al2O3) * Ar (Al) * 100% / Mr (Al2O3) = 2 * 27 * 100% / 102 = 52,94%;
ω (O в Al2O3) = 100% - ω (Al в Al2O3) = 100% - 52,94% = 47,06%
3.
CH4 (g) + 2 O2 (g) → 2 H2O (l) + CO2
2 ZnS + 3 O2 → 2 SO2 + 2 ZnO
Объяснение:
Дано:
m(C₁₂H₂₂O₁₁) = 342 гр
Найти:
N(AТФ) - ?
1) Сахароза – дисахарид и состоит из α-D-глюкозы и β-D-фруктозы, их энергетическая ценность при окислении одинакова.
C₁₂H₂₂O₁₁ + H₂O (H⁺ , t°C)→ C₆H₁₂O₆ + C₆H₁₂O₆
Сахароза α-D-глюкоза β-D-фруктоза
2) Для начала мы найдем молекулярную массу сахарозы, а потом находим количества молекул у сахарозы а потом у глюкозы:
M(C₁₂H₂₂O₁₁) = 12×12 + 1×22 + 16×11 = 144 + 22 + 176 = 342 гр/моль
n(C₁₂H₂₂O₁₁) = m(C₁₂H₂₂O₁₁)/M(C₁₂H₂₂O₁₁) = 342 гр / 342 гр/моль = 1 моль ⇒ n(C₆H₁₂O₆) = n(C₁₂H₂₂O₁₁) = 1 моль
3) Теперь находим количества вещества у сахарозы:
N(C₁₂H₂₂O₁₁) = n(C₁₂H₂₂O₁₁)×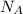 = 1 моль × 6,02×10²³ (моль)⁻¹ = 6,02×10²³ молекул
= 1 моль × 6,02×10²³ (моль)⁻¹ = 6,02×10²³ молекул
4) Теперь найдем сколько молекул АТФ образовалось в результате анаэробного и аэробного условия, зная что в результате анаэробного условия образуется 3 молекулы АТФ, а в результате аэробного условия 38 молекул (в расчёте на 1 молекулу глюкозы):
N(АТФ) = n(АТФ)×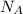 = 3 моль × 6,02×10²³ (моль)⁻¹ = 18,06×10²³ молекул - при анаэробном условий.
= 3 моль × 6,02×10²³ (моль)⁻¹ = 18,06×10²³ молекул - при анаэробном условий.
N(АТФ) = n(АТФ)×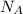 = 38 моль × 6,02×10²³ (моль)⁻¹ = 228,76×10²³ молекул - при аэробном условий.
= 38 моль × 6,02×10²³ (моль)⁻¹ = 228,76×10²³ молекул - при аэробном условий.
ответ: N(АТФ) = 18,06×10²³ молекул - при анаэробном условий.
N(АТФ) = 228,76×10²³ молекул - при аэробном условий.
Решено от :