Хлоридна кислота яка міститься в 50 г розчину з масовою часткою хлороводню 14,6%, повнiстю прореагувала з алюминием обчислiть масу солi, яка утворилася пiд час реакцii
ответ: ответ ниже. "⇒" и "=" заменить на стандартную "стрелочку" в химии.
Объяснение:
159) a)N( Степень окисления была -3, так как азот связан с тремя водородами, степень окисления которых равна +1) ⇒ N (степень окисления +2, так как связан с кислородом, степень окисления которого равна -2) ; Было -3, а стало +2, значит, N отдал 5 электрона.
б) O ( в 0 степени окисления, так как не связан больше ни с каким элементом) ⇒ O ( - 2 степень окисления, так как связан с двумя водородами, чья степень окисления равна +2) ; Было 0, а стало -2, значит, O получил 2 электрона.
(1-(окисление азота) и (восстановление кислорода)
Там 5 электронов, а здесь 2 электрона. Приводим к наименьшему общему кратному, домножая первую часть уравнения на 2, а вторую - на 5. Получаем (К окислителю 2, к восстановителю 5) . В молекулярной форме это будет : 4NH3+5O2 ⇒ 4NO2 + 6H2O.
В 161 всё аналогично. Сразу перейду к коэффициентам
,( к окислению идёт коэффициент 2, а к восстановителю 3), что в молекулярной формуле 4NH3+3O2⇒ 2N2 + 6 H2O
ответ: ответ ниже. "⇒" и "=" заменить на стандартную "стрелочку" в химии.
Объяснение:
159) a)N( Степень окисления была -3, так как азот связан с тремя водородами, степень окисления которых равна +1) ⇒ N (степень окисления +2, так как связан с кислородом, степень окисления которого равна -2) ; Было -3, а стало +2, значит, N отдал 5 электрона.
б) O ( в 0 степени окисления, так как не связан больше ни с каким элементом) ⇒ O ( - 2 степень окисления, так как связан с двумя водородами, чья степень окисления равна +2) ; Было 0, а стало -2, значит, O получил 2 электрона.
Там 5 электронов, а здесь 2 электрона. Приводим к наименьшему общему кратному, домножая первую часть уравнения на 2, а вторую - на 5. Получаем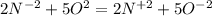 (К окислителю 2, к восстановителю 5) . В молекулярной форме это будет : 4NH3+5O2 ⇒ 4NO2 + 6H2O.
(К окислителю 2, к восстановителю 5) . В молекулярной форме это будет : 4NH3+5O2 ⇒ 4NO2 + 6H2O.
В 161 всё аналогично. Сразу перейду к коэффициентам
m(H2O)=500 г 2Fe+3Cl2=>2FeCl3
m(Fe)=22.4 г n(Cl2)=
v(Cl2)=15.68 л n(Fe)=
w(FeCl3)=?
m(раствора)=m(FeCl3)+m(H2O)=65+500=565 г
w=
2) ДАНО: РЕШЕНИЕ:
m(Na2CO3)=53г Na2CO3+2HNO3=>2NaNO3+H2O+CO2
m(раствор HNO3)=400г m(HNO3)=w(HNO3)*m(раствор HNO3)=0.2*400=80 г
w(раствор HNO3)=20% n(HNO3)=
V(CO2)=? n(Na2CO3)=
HNO3 - в избытке => расчет ведется по Na2CO3
3) ДАНО: РЕШЕНИЕ:
m(N2)=50г 3H2+N2=>2NH3
w(примесь)=5% n(N2)=m(N2)/M(N2)=5.6/28=0.2 моль
m(NH3)=8г n(NH3)=0.4 моль
w(NH3)=? mтеор.(NH3)=n*M=17*0.4=6.8 г
w(NH3)=mпрактическая/mтеоретическая= 5/6.8=0.74