К60 г 60%-ного раствора нитрита серебра добавили 40 мл воды. массовая доля нитрата серебра в полученном растворе равна % минимальное количество вещества серной кислоты, необходимое для получения 11,2 л водорода .
1. а) сначала необходимо найти массу нитрата в первом растворе:
m(AgNO3)=m1(раствора)*w1(AgNO3)=60*0,6=36 г
б) теперь определим массу нового раствора,после добавления воды:
m2(раствора)=m1(растворара)+m(H2O)=60+40=100 г(г с мл смешивать нельзя,но учитывая,что плотность воды равна 1 г/мл,поэтому 40 мл численно равно 40 г воды)
в)теперь,отнеся массу соли(так как она не изменилась) к массе нового раствора и получим вторую массовую долю:
w2(AgNO3)=m(AgNO3)/m2(раствора)=36/100=0,36 или 36%
х моль 11,2 л
2. →
1 моль 22,4 л
При взаимодействии 1 моль кислоты выделяется 22,4 л водорода, а
при -- // -- х моль___________________11,2 л, откуда
1. а) сначала необходимо найти массу нитрата в первом растворе:
m(AgNO3)=m1(раствора)*w1(AgNO3)=60*0,6=36 г
б) теперь определим массу нового раствора,после добавления воды:
m2(раствора)=m1(растворара)+m(H2O)=60+40=100 г(г с мл смешивать нельзя,но учитывая,что плотность воды равна 1 г/мл,поэтому 40 мл численно равно 40 г воды)
в)теперь,отнеся массу соли(так как она не изменилась) к массе нового раствора и получим вторую массовую долю:
w2(AgNO3)=m(AgNO3)/m2(раствора)=36/100=0,36 или 36%
х моль 11,2 л
2.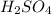 →
→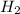
1 моль 22,4 л
При взаимодействии 1 моль кислоты выделяется 22,4 л водорода, а
при -- // -- х моль___________________11,2 л, откуда
х=1*11,2/22,4=0,5 моль