Какова массовая доля серной кислоты в растворе (в %), 250 г которого вступают во взаимодействие с избытком гидроксида натрия с образованием 56,8 г соли. ответ запишите числом с точностью до сотых, без единицы измерения, пробелов и знаков препинания. Например: 13,67
1) В пределах одной группы металлические свойства возрастают при увеличении порядкового номера элемента. Это связано с увеличением радиуса атома и более легким отхождением электронов от ядра.
ОТВЕТ: а)
2) Имея только один электрон на внешнем энергетическом уровне, элемент может иметь валентность только 1, соответственно может содержать только одну ОН группу и два атома на кислород в окисде.
ОТВЕТ: в)
3) Как уже было сказано в первом номере, в одной группе радиус атома увеличивается с увеличением его порядкового номера.
ОТВЕТ: г)
4) Щелочные металлы невероятно активны, и всячески стремятся перейти в устойчивую для себя форму иона, с зарядом +1. Поэтому в свободной форме в природе не встречаются и окислительных свойств не проявляют почти совсем, а восстановительных в степени окисления +1 в принципе не могут проявлять, но что правда про них, это то, что их действительно почти все можно спокойно резать ножом и намазывать на хлеб, главное потом не есть)
ОТВЕТ: в)
5) Реакция натрия с водой невероятно экзотермична. Натрий как бешеный носится по поверхности и искрит. В то же время это является реакцией замещения водорода на натрий. Продуктом реакции является щелочь.
ОТВЕТ: в)
6) Основные свойства щелочей тем выше, чем активнее металл, входящий в соединение наиболее активным металлом является литий.
ОТВЕТ: а)
7) С раствором щелочи точно не могут взаимодействовать основные соединения. Могут лишь кислотные и амфотерные. Могут таже растворимые соли, если в результате реакции получается нерастворимвый гидроксид.
ОТВЕТ: б)
8) Соли натрия содержает его ионы. Ионы натрия окрашивают пламя горелки в желтый цвет.
ОТВЕТ: г)
9) Каустическая сода (она же едкий натр) - тривиальное название гидроксида натрия
ОТВЕТ: в)
10) Хлорид соединие вида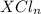 , сульфид
, сульфид 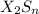 , гидрид
, гидрид 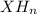 .
.
ОТВЕТ: в)
1. 2KOH+SO3=H2O+K2SO4 (сульфат калия + малодиссоциирующее в-во (вода))
2. Cu(OH)2=CuO+H2O (оксид меди 2 + вода, реакция идет при нагревании)
3. 2K+H2O=K2O+H2 (оксид калия + водород)
4. Ca(OH)2+Na2CO3=2NaOH+CaCO3 (гидроксид натрия + карбонат кальция)
5. 2KOH+Na2CO3=2NaOH+K2CO3 (гидроксид натрия + карбонат калия) ps вообще, эта реакция не может идти, т к нет ни малодиссоциирующего в-ва, ни осадка, ни газа... ну если надо, то держите.
6. 3LiOH+Na3PO4=Li3PO4+3NaOH (фосфат лития + гидроксид натрия)
7. Fe(OH)2+H2SO4=FeSO4+2H2O (сульфат железа 2 + вода)
8. 2Na+H2O=Na2O+H2 (оксид натрия + водород)
9. 6KOH+P2O5=2K3PO4+3H2O (фосфат калия + вода)
10. Ca(OH)2+CO2=CaCO3+H2O (карбонат кальция + вода)
11.Fe(OH)2=FeO+H2O (оксид железа 2 + вода (реакция протекает при нагревании))
12. 2LiOH+SO3=LiSO4+H2O (сульфат лития + вода)
13. Ca+H2O=CaO+H2 (оксид кальция + водород)
14. 2KOH+CuSO4=Cu(OH)2+K2SO4 (гидроксид меди 2 + сульфат калия)
15. Fe(OH)2+2HNO3=Fe(NO3)2+2H2O (нитрат железа 2 + вода)
16. 2LIOH+H2SO4=Li2SO4+2H2O (сульфат лития + вода)
17. Cu(OH)2+2HNO3=Cu(NO3)2+2H2O (нитрат меди 2 + вода)
18. Ba+H2O=BaO+H2 (оксид бария + вода)
19. Ba(OH)2+CO2=BaCO3+H2O (карбонат бария + вода)
Объяснение: