CuSO₄ +2NaOH = Cu(OH)₂ + 2NaSO₄
C₆H₁₂O₆ + 2Cu(OH)₂ = С₂H₁₂O₇ + Cu₂O + 2H₂O
1) Найдем массу сульфата меди, участвовавшего в реакции:
ω=m(вещества)÷m(раствора)×100% ⇒ m(вещества)=ω×m(раствора)÷100%
m(CuSO₄)=40 г
2) Найдем массу образовавшегося осадка Cu(OH)₂:
M(CuSO₄)= 160 г/моль
M(Cu(OH)₂)= 98 г/моль
m(CuSO₄)= 40 г
m(Cu(OH)₂)= х г
160 г CuSO₄ дают 98 г Cu(OH)₂
40 г CuSO₄ дают х г Cu(OH)₂
24,5 г Cu(OH)₂
3) Определим сколько глюкозы потребовалось для реакции с гидроксидом меди:
M(C₆H₁₂O₆)= 180 г/моль
m(Cu(OH)₂)= 24,5 г
m(C₆H₁₂O₆)= у г
98 г Cu(OH)₂ прореагировало с 180 г C₆H₁₂O₆
24,5 г Cu(OH)₂ прореагировало с у г C₆H₁₂O₆
45 г C₆H₁₂O₆
4) Расчитаем массу 10%-ного раствора:
ω=m(вещества)÷m(раствора)×100% ⇒ m(раствора)=m(вещества)÷ω×100%
m(раствора)=450 г
5) Найдем объем раствора через плотность:
⇒
V(C₆H₁₂O₆)=500 мл
ответ: потребуется взять 500 мл 10% раствора глюкозы.
CuSO₄ +2NaOH = Cu(OH)₂ + 2NaSO₄
C₆H₁₂O₆ + 2Cu(OH)₂ = С₂H₁₂O₇ + Cu₂O + 2H₂O
1) Найдем массу сульфата меди, участвовавшего в реакции:
ω=m(вещества)÷m(раствора)×100% ⇒ m(вещества)=ω×m(раствора)÷100%
m(CuSO₄)=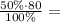 40 г
40 г
2) Найдем массу образовавшегося осадка Cu(OH)₂:
M(CuSO₄)= 160 г/моль
M(Cu(OH)₂)= 98 г/моль
m(CuSO₄)= 40 г
m(Cu(OH)₂)= х г
160 г CuSO₄ дают 98 г Cu(OH)₂
40 г CuSO₄ дают х г Cu(OH)₂
3) Определим сколько глюкозы потребовалось для реакции с гидроксидом меди:
M(Cu(OH)₂)= 98 г/моль
M(C₆H₁₂O₆)= 180 г/моль
m(Cu(OH)₂)= 24,5 г
m(C₆H₁₂O₆)= у г
98 г Cu(OH)₂ прореагировало с 180 г C₆H₁₂O₆
24,5 г Cu(OH)₂ прореагировало с у г C₆H₁₂O₆
4) Расчитаем массу 10%-ного раствора:
ω=m(вещества)÷m(раствора)×100% ⇒ m(раствора)=m(вещества)÷ω×100%
m(раствора)=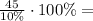 450 г
450 г
5) Найдем объем раствора через плотность:
V(C₆H₁₂O₆)=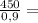 500 мл
500 мл
ответ: потребуется взять 500 мл 10% раствора глюкозы.