Контрольная работа по теме Металлы 9 класс
3-й вариант
1. Металлические свойства элементов 2 периода с увеличением порядкового номера:
1) убывают; 2) возрастают; 3) не изменяются; 4) меняются периодически.
2.Щелочные металлы находятся в: А) IА группе; Б) IIА группе; В) IБ группе; Г) IIБ группе.
3.Распределение электронов по энергетическим уровням в атоме натрия:
1) 2е, 3е; 2) 2е, 1е; 3) 2е; 4е; 4) 2е, 8е, 1е.
4..Атоммагния отличается от иона магния:
а) зарядом ядра б) зарядом частицы в) числом протонов г) числом нейтронов
5.При комнатной температуре с водой взаимодействуют оба металла:
1)калий и медь; 2) алюминий и магний; 3) натрий и кальций; 4) олово и цинк.
6.Металл с наиболее ярко выраженными металлическими свойствами:
1) Be; 2) Ba; 3) Mg; 4) Ca.
7.Если продукты в реакции сульфат алюминия и вода, то исходными веществами являются:
1)алюминий и серная кислота; 2) оксид алюминия и оксид серы (VI)
3) гидроксид алюминия и серная кислота; 4) алюминий и вода.
8..Гидрооксид цинка взаимодействует с веществом, формула которого:
а)KOH б) KNO3(p-p) в)NaCI(p-p) г)BaSO4
9.Барий взаимодействует с:
А) Сl2; В) NaCl ; Б) Mg; Г) H2O.
10.Установите соответствие между реагентами и продуктами реакции:
РЕАГЕНТЫ ПРОДУКТЫ
А) Al + Cl2 1) NaAlO2 + H2O
Б) Al + H2SO4(р) 2) Al2(SO4)3 + H2
В) Al(OH)3 + NaOH3) Al2(SO4)3 + H2O
Г) Al(OH)3+ H2SO4 4) AlCl3
Часть Б
11.Напишите уравнения реакций по схеме превращений, определите тип реакции.
Ba(NO3)2Ba → BaO → Ba(OH)2 → BaCl2→ВаSO4
12.Даны растворы: NaCI, FeCI2,FeCI3Как определить, где какое вещество находится? Написать уравнения реакций.
13. Как используя любые реактивы и барий получить оксид, основание, соль. Составьте уравнения реакций в молекулярном виде.(3б)
14.Какой объем водорода выделится при взаимодействии магния с 100 г раствора серной кислоты, с массовой долей кислоты в растворе, равной 24,5%
2,2,3,3,4-пентаметилпентан 2,2,3,3-тетраметилгексан 2,2,3,4,4-пентаметилпентан 2,2,3,4-тетраметилгексан 2,2,3,5-тетраметилгексан 2,2,3-триметил-3-этилпентан 2,2,3-триметилгептан 2,2,4,4-тетраметилгексан 2,2,4,5-тетраметилгексан 2,2,4-триметил-3-этилпентан 2,2,4-триметилгептан 2,2,5,5-тетраметилгексан 2,2,5-триметилгептан 2,2,6-триметилгептан 2,2-диметил-3-этилгексан 2,2-диметил-4-этилгексан 2,2-диметилоктан 2,3,3,4-тетраметилгексан 2,3,3,5-тетраметилгексан 2,3,3-триметилгептан 2,3,4,4-тетраметилгексан 2,3,4-триметил-3-этилпентан 2,3,4-триметилгептан 2,3,5-триметилгептан 2,3,6-триметилгептан 2,3-диметил-3-этилгексан 2,3-диметил-4-этилгексан 2,3-диметилоктан 2,4,4-триметилгептан 2,4,5-триметилгептан 2,4,6-триметилгептан 2,4-диметил-3-этилгексан 2,4-диметил-4-этилгексан 2,4-диметилоктан 2,5,5-триметилгептан 2,5-диметил-3-этилгексан 2,5-диметилоктан 2,6-диметилоктан 2,7-диметилоктан 2-метил-3,3-диэтилпентан 2-метил-3-этилгептан 2-метил-4-этилгептан 2-метил-5-этилгептан 2-метилнонан 3,3,4,4-тетраметилгексан 3,3,4-триметилгептан 3,3,5-триметилгептан 3,3-диметил-4-этилгексан 3,3-диметилоктан 3,3-диэтилгексан 3,4,4-триметилгептан 3,4,5-триметилгептан 3,4-диметил-3-этилгексан 3,4-диметилоктан 3,4-диэтилгексан 3,5-диметилоктан 3,6-диметилоктан 3-изопропил-2,4-диметилпентан 3-изопропил-2-метилгексан 3-метил-3-этилгептан 3-метил-4-этилгептан 3-метил-5-этилгептан 3-метилнонан 3-этилоктан 4,4-диметилоктан 4,5-диметилоктан 4-изопропилгептан 4-метил-3-этилгептан 4-метил-4-этилгептан 4-метилнонан 4-пропилгептан 4-этилоктан 5-метилнонан н-декан
Источник: https://gomolog.ru/baza-znanii/strukturnye-formuly/2,3,4,5-tetrametilgeksan.html
Объяснение:
1. Докажите опытным путём состав: а) гидроксида кальция; б) сульфата аммония.
а) Проведём качественную реакцию на гидроксид-ион. Для этого воспользуемся индикаторами. Гидроксид кальция - основание малорастворимое, но тем не менее некоторое количество растворяется, следовательно среду изменять будет. Возьмём индикатор фенолфталеин, добавим его в пробирку с гидроксидом кальция, в результате раствор частично изменит цвет на малиновый - следовательно среда щелочная (слабощелочная).
б) Проведём качественную реакцию на сульфат-ион. Для этого возьмём любую растворимую соль бария (по стандарту - хлорид бария), добавим его в раствор с сульфатом аммония. В ходе реакции выпадает белый осадок - сульфат бария. Реакция выглядит следующим образом:
ᅠᅠ
2. Испытайте растворы нитрата натрия, карбоната натрия и нитрата цинка раствором индикатора или индикаторной бумагой, и объясните результаты испытаний. Запишите молекулярные и ионные уравнения реакций гидролиза:
1. Нитрат натрия - соль, образованная сильным основанием NaOH и сильной кислотой HNO₃, гидролиз протекать не будет, среда нейтральная. Это можно доказать следующим путём: возьмём индикатор метиловый оранжевый, добавим его в раствор нитрата натрия, в результате цвет изменится на оранжевый. Это и есть признак нейтральной среды.
2. Карбонат натрия - соль, образованная сильным основанием NaOH и слабой кислотой H₂CO₃. Гидролиз протекает по аниону, образующаяся среда - щелочная, гидролиз обратимый, протекает в две стадии:
ᅠᅠ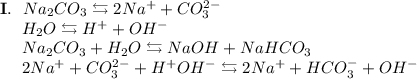
ᅠᅠ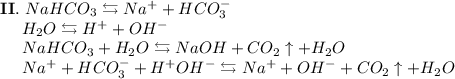
Добавим в раствор метиловый оранжевый. Раствор поменяет цвет на жёлтый, следовательно реакция среды щелочная.
3. Нитрат цинка - соль, образованная слабым основанием Zn(OH)₂ и сильной кислотой HNO₃. Гидролиз протекает по катиону, образующаяся среда - кислая, гидролиз обратимый, протекает в две стадии:
ᅠᅠ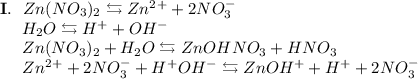
ᅠᅠ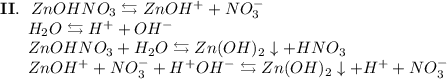
Добавим в раствор метиловый оранжевый. Раствор поменяет цвет на красный, следовательно реакция среды кислая.
3. Практически осуществите все следующие превращения: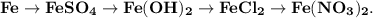
1. Получим сульфат железа путём реакции железа и разбавленной серной кислоты:
ᅠᅠ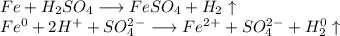
С точки зрения ОВР:
ᅠᅠ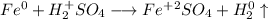
ᅠᅠ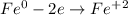 | 2 | 1 | окисление
| 2 | 1 | окисление
ᅠᅠ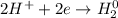 | 2 | 1 | восстановление
| 2 | 1 | восстановление
ᅠᅠFe - восстановитель, H₂SO₄ (2H⁺) - окислитель.
2. Получим гидроксид железа путём реакции сульфата железа и гидроксида калия:
ᅠᅠ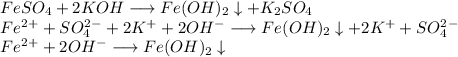
3. Получим хлорид железа путём реакции гидроксида железа и хлороводородной кислоты:
ᅠᅠ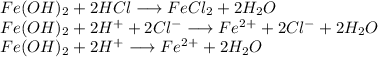
4. Получим нитрат железа путём реакции хлорида железа и азотной кислоты: