1. Найдем через плотность относительную молекулярную формулу вещества:
2. Теперь,вспомнив формулу по вычислению массовой доли элемента в веществе и выведя из нее n - количество атомов элемента,найдем количество атомов каждого:
P.S. - в некоторых ионах(например Н¹⁺, К¹⁺ и др.) я пишу перед знаком заряда единицу. Единица на самом деле не пишется, пишется просто + или -. Но если без единицы, то знак почему-то не отображается. И вместо него квадраты. Поэтому, когда будите переписывать в тетрадь, то просто пишите + или - без единицы.
1. Найдем через плотность относительную молекулярную формулу вещества:
2. Теперь,вспомнив формулу по вычислению массовой доли элемента в веществе и выведя из нее n - количество атомов элемента,найдем количество атомов каждого:
а) n(C)=Mr(C_xH_yO_z)*w(C)/Ar(C)*100%=72*66,67/12*100=4
б) n(H)=Mr(C_xH_yO_z)*w(H)/Ar(H)*100%=72*11,11/1*100=8
в) n(O)=Mr(C_xH_yO_z)*w(O)/Ar(O)*100%=72*22,22/16*100=1
Выходит простейшая формула: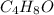
Если подставлять в общие формулы кислородсодержащих соединений,то получим: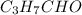 -это бутаналь
-это бутаналь
1) Al₂(SO₄)₃ = 2Al³⁺ + 3SO₄²⁻ (алюминат-ион, сульфат-ион).
2) K₂CO₃ = 2K¹⁺ + CO₃²⁻ ( ион калия, карбонат-ион).
3) (NH₄)₃PO₄ = 3NH₄⁺ + PO₄³⁻ ( ион аммония, фосфат-ион).
4) Cu(NO₃)₂ = Cu²⁺ + 2NO₃ (ион меди, нитрат-ион).
5) Ba(OH)₂ = Ba²⁺ + 2OH¹⁻ (ион бария, гидроксид-ион).
6) HCl = H¹⁺ Cl¹⁻ (ион водорода, хлорид-ион).
7) KOH = K¹⁺ + OH¹⁻ (ион калия, гидроксид-ион).
8) AlCl₂ = Al²⁺ + 2Cl¹⁻ (аллюминат-ион, хлорид-ион).
P.S. - в некоторых ионах(например Н¹⁺, К¹⁺ и др.) я пишу перед знаком заряда единицу. Единица на самом деле не пишется, пишется просто + или -. Но если без единицы, то знак почему-то не отображается. И вместо него квадраты. Поэтому, когда будите переписывать в тетрадь, то просто пишите + или - без единицы.