Оксид элемента x обработан соляной кислотой,при этом образовалась соль xcl3 . массовая доля хлорид-ионов в составе соли 65,5%. установите элемент х, запишите формулу названного оксида и уравнение реакции его с соляной кислотой.
какой массы простое вещество, образованное элементом х,можно получить из руды массой 500кг ,основным компонентом которой является указанный оксид если массовай доля примесей в руде составляет 12%
M(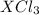 )=M(X)+35.5*3=M(X)+106.5
)=M(X)+35.5*3=M(X)+106.5
M(X)=56г/моль что соответствует железу
m(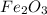 )=500000*0.88=440000г
)=500000*0.88=440000г
n(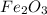 )=440000/160=2750моль
)=440000/160=2750моль
n(Fe)=2750*2=5500моль
m(Fe)=5500*56=308кг