Посчитаем кол-во в-ва NaF (оно равно массе деленной на молярную массу )
Так как кол-во в-ва NaF и HF равны, найдем массу HF (они равны, так как равны коэффициенты при формулах в уравнении реакции, это стехиометрический закон)
Процентная концентрация равна массе в-ва / массу р-ра ( практически тоже, что и массовая доля, масса раствора равна сумме массы растворителя, в нашем случае воды (100г), и растворенного в-ва, в нашем случае плавиковой кислоты HF (15г), то есть в сумме 115г)
Металлический алюминий реагирует с кислородом с образованием окиси алюминия. Реакция описывается следующим уравнением химической реакции:
4Al + 3O2 = 2Al2O3;
Посчитаем химическое количество алюминия. Для этого поделим массу имеющегося вещества на его молярный вес.
М Al = 27 грамм/моль;
N Al = 8,1 / 27 = 0,3 моль;
При сжигании алюминия на 1 моль металла необходимо взять ¾ = 0,75 моль кислорода. Найдём его объем.
С этой целью умножим количество кислорода на объем 1 моля газа (составляющий 22,4 литра).
N О2 = 0,3 / 4 х 3 = 0,225 моль;
V O2 = 0,225 х 22,4 = 5,04 литра;
C = 13%
Объяснение:
Запишем уравнение реакции получения HF из NaF
Посчитаем кол-во в-ва NaF (оно равно массе деленной на молярную массу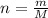 )
)
Так как кол-во в-ва NaF и HF равны, найдем массу HF (они равны, так как равны коэффициенты при формулах в уравнении реакции, это стехиометрический закон)
Процентная концентрация равна массе в-ва / массу р-ра (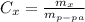 практически тоже, что и массовая доля, масса раствора равна сумме массы растворителя, в нашем случае воды (100г), и растворенного в-ва, в нашем случае плавиковой кислоты HF (15г), то есть в сумме 115г)
практически тоже, что и массовая доля, масса раствора равна сумме массы растворителя, в нашем случае воды (100г), и растворенного в-ва, в нашем случае плавиковой кислоты HF (15г), то есть в сумме 115г)