цинковая пластинка погружена в раствор ZnSO4, а медная пластинка - в раствор CuSO4. Полуэлементы соединены ионным мостиком.
При замыкании внешней цепи IV на аноде происходит окисление цинка:
Zn - 2е = Zn2+
На катоде - восстановление ионов меди:
Cu2+ + 2е = Cu
За счет окислительно-восстановительной реакции по внешней цепи течет поток электронов от цинкового электрода к медному, а по ионному мостику движутся сульфат-ионы. Цинковый электрод постепенно растворяется, на медном выделяется металлическая медь. Схеме элемента запишется так:
Здесь у нас довольно необычная ОВР - два сильнейших окислителя - кислород и фтор. Но все - таки, кислород будет восстановителем, ибо фтор ни при каких условия не будет таковым.
Запишем данную реакцию вместе со степенями окисления:
Запишем реакции окисления и восстановления. Окисляться у нас будет кислород, так как степень окисления у него растет от -2 до +2(во фториде ), запишем этот процесс:
- окисление, кислород - восстановитель
Теперь со фтором. Фтор - самый сильный - ПЕРВЫЙ окислитель, у никогда не будет положительной степени окисления. В этой реакции его СО изменяется от 0 до -1. Запишем этот переход:
- восстановление - сам фтор - окислитель
Теперь распишем переходы электронов для каждого процесса:
Для Фтора:
- теперь уравняем фтор, что бы и слева и справа его было по 2:
Для Кислорода:
- здесь все нормально.
Теперь нам надо, чтобы количество оттданых элетронов(т.е. число электронов которые отдал кислород) равнялось количеству принятых электронов(т.е. тех которые принял фтор). Кислород отда - 4 электрона, а фтор принял только - 2, значит уравнение восстановления фтора умножаем на два:
Теперь мы суммируем, т.е. записываем в систему два полученных уравнения с кислородом и со фтором:
- восстановление - окислитель
- окисление - восстановитель.
Та двойка которая получилась перед и та 4 которая получилась перед - это коэффициенты - выносим их в левую часть получим:
- видим, что фтора - 4, а в правой части только три, значит нам надо поставить перед - двойку. Поулчим:
- теперь натрий обделили, в левой части - 1, а в правой - 2, значит нам надо поставить 2 перед , перепишем с получившимися коэффициентами:
цинковая пластинка погружена в раствор ZnSO4, а медная пластинка - в раствор CuSO4. Полуэлементы соединены ионным мостиком.
При замыкании внешней цепи IV на аноде происходит окисление цинка:
Zn - 2е = Zn2+
На катоде - восстановление ионов меди:
Cu2+ + 2е = Cu
За счет окислительно-восстановительной реакции по внешней цепи течет поток электронов от цинкового электрода к медному, а по ионному мостику движутся сульфат-ионы. Цинковый электрод постепенно растворяется, на медном выделяется металлическая медь. Схеме элемента запишется так:
анод(-) Zn | ZnSO4 CuSO4 | Cu катод(+)
Здесь у нас довольно необычная ОВР - два сильнейших окислителя - кислород и фтор. Но все - таки, кислород будет восстановителем, ибо фтор ни при каких условия не будет таковым.
Запишем данную реакцию вместе со степенями окисления:
Запишем реакции окисления и восстановления. Окисляться у нас будет кислород, так как степень окисления у него растет от -2 до +2(во фториде ), запишем этот процесс:
Теперь со фтором. Фтор - самый сильный - ПЕРВЫЙ окислитель, у никогда не будет положительной степени окисления. В этой реакции его СО изменяется от 0 до -1. Запишем этот переход:
Теперь распишем переходы электронов для каждого процесса:
Для Фтора:
Для Кислорода:
Теперь нам надо, чтобы количество оттданых элетронов(т.е. число электронов которые отдал кислород) равнялось количеству принятых электронов(т.е. тех которые принял фтор). Кислород отда - 4 электрона, а фтор принял только - 2, значит уравнение восстановления фтора умножаем на два:
Теперь мы суммируем, т.е. записываем в систему два полученных уравнения с кислородом и со фтором:
Та двойка которая получилась перед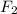 и та 4 которая получилась
и та 4 которая получилась  перед - это коэффициенты - выносим их в левую часть получим:
перед - это коэффициенты - выносим их в левую часть получим:
Понятно???