Получение и свойства оксидов. - тонкую ленточку магния зажать в тигельных щипцах и внести пламя спиртовки. продукт горения собрать в пробирку, добавить немного воды и 2-3 капли финолфталеина. написать уравнение реакций, наблюдение
Допустим воды для растворения много. Тогда нерастворимый осадок 3,5 г это карбонат кальция. Значит сразу считаем его процент 3,5/10 = 0,35 или 35%. Идем дальше. Пишем обе возможные реакции. CaCO3 = CaO + CO2 2NaHCO3 = Na2CO3 + H2O + CO2 (или проще для расчетов будет записать Na2CO3 + H2CO3). Если есть 20 г смеси, то в ней 20*0,35 = 7 грамм нашего карбоната, а значит 7/100 = 0,07 моль. Столько же моль и углекислого газа, который выделяется при его разложении, а значит масса газа = 0,07*44 = 3,08 г. Вычитаем эту цифру из 5,2-3,08 = 2,12 грамма, а это и есть наша H2CO3. Считаем количество угольной кислоты 2,12/62 = 0,034 моль. По реакции Na2CO3 в 2 раза больше = 0,068. Считаем массу NaHCO3 0,068*84 = 5,712 грамм. Считаем массу BaCl2 20-(7+5.712) = 7.288 грамма. Ну и дело за процентами CaCO3 = 35% NaHCO3 = 5.712/20 ≈ 0.29 или 29% BaCl2 = 7.288/20 ≈ 0.36 или 36%
Составим уравнение и подпишем под ним то, что дано:
С₂Н₅ОН + Na => C₂H₅ONa + H₂↑
69 г х г
m (Na) = M×n
m (Na) = 22,98 г\моль 1 моль= 22,98 грамм.
m (H₂) = M×n
m (H₂) = 1 г\моль ×2 моль= 2 грамма
Составляем пропорцию:
69 г (Na) - х г (H₂)
22,98 г (Na) - 2 г (H₂)
Отсюда =>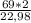 = 6,005 грамм.
= 6,005 грамм.
ответ: 6,005 грамм
Объяснение:
Т.к в уравнении мы имеем один Na, и зная его молярную массу из таблицы Менделеева 22,98 г\моль, то можем найти его массу:
m (Na) = M×n
m (Na) = 22,98 г\моль 1 моль= 22,98 грамм.
Аналогично находим массу водорода
В уравнении у нас H₂, значит количество водорода n=2 моль, молярная масса M(H) = 1 г\моль
m (H₂) = M×n
m (H₂) = 1 г\моль ×2 моль= 2 грамма
Идем дальше. Пишем обе возможные реакции.
CaCO3 = CaO + CO2
2NaHCO3 = Na2CO3 + H2O + CO2 (или проще для расчетов будет записать Na2CO3 + H2CO3).
Если есть 20 г смеси, то в ней 20*0,35 = 7 грамм нашего карбоната, а значит 7/100 = 0,07 моль. Столько же моль и углекислого газа, который выделяется при его разложении, а значит масса газа = 0,07*44 = 3,08 г.
Вычитаем эту цифру из 5,2-3,08 = 2,12 грамма, а это и есть наша H2CO3. Считаем количество угольной кислоты 2,12/62 = 0,034 моль. По реакции Na2CO3 в 2 раза больше = 0,068. Считаем массу NaHCO3 0,068*84 = 5,712 грамм. Считаем массу BaCl2 20-(7+5.712) = 7.288 грамма.
Ну и дело за процентами
CaCO3 = 35%
NaHCO3 = 5.712/20 ≈ 0.29 или 29%
BaCl2 = 7.288/20 ≈ 0.36 или 36%