Составим уравнение и подпишем под ним то, что дано:
С₂Н₅ОН + Na => C₂H₅ONa + H₂↑
69 г х г
m (Na) = M×n
m (Na) = 22,98 г\моль 1 моль= 22,98 грамм.
m (H₂) = M×n
m (H₂) = 1 г\моль ×2 моль= 2 грамма
Составляем пропорцию:
69 г (Na) - х г (H₂)
22,98 г (Na) - 2 г (H₂)
Отсюда => = 6,005 грамм.
ответ: 6,005 грамм
Объяснение:
Т.к в уравнении мы имеем один Na, и зная его молярную массу из таблицы Менделеева 22,98 г\моль, то можем найти его массу:
Аналогично находим массу водорода
В уравнении у нас H₂, значит количество водорода n=2 моль, молярная масса M(H) = 1 г\моль
9,5 л
m(чистого Ca) = 18 г (1 - 0,02) = 17,64 г
n(Ca) = 17,64 г / 40 г/моль = 0,441 моль
Реакция с серной кислотой:
Ca + H₂SO₄ = CaSO₄ + H₂
n(прореаг H₂SO₄) = 0,441 моль
Сделаем вывод об избытке/недостатке серной кислоты:
m(H₂SO₄) = 80 г * 0,4 = 32 г
n(H₂SO₄) = 32 г / 98 г/моль = 0,327 моль
Следовательно, кислота в недостатке и n(прореаг с H₂SO₄ Ca) = 0,327 моль
Оставшийся кальций реагирует с водой:
Ca + 2H₂O = Ca(OH)₂ + H₂
Но мы видим, что в любом случае n(H₂) = n(Ca) = 0,441 моль
V(H₂) = 0,441 моль * 22,4 л/моль = 9,88 л
Но это лишь теоретический выход. Практический выход составляет 96%:
V(практический выход H₂) = 9,88 л * 0,96 ≅ 9,5 л
Составим уравнение и подпишем под ним то, что дано:
С₂Н₅ОН + Na => C₂H₅ONa + H₂↑
69 г х г
m (Na) = M×n
m (Na) = 22,98 г\моль 1 моль= 22,98 грамм.
m (H₂) = M×n
m (H₂) = 1 г\моль ×2 моль= 2 грамма
Составляем пропорцию:
69 г (Na) - х г (H₂)
22,98 г (Na) - 2 г (H₂)
Отсюда =>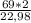 = 6,005 грамм.
= 6,005 грамм.
ответ: 6,005 грамм
Объяснение:
Т.к в уравнении мы имеем один Na, и зная его молярную массу из таблицы Менделеева 22,98 г\моль, то можем найти его массу:
m (Na) = M×n
m (Na) = 22,98 г\моль 1 моль= 22,98 грамм.
Аналогично находим массу водорода
В уравнении у нас H₂, значит количество водорода n=2 моль, молярная масса M(H) = 1 г\моль
m (H₂) = M×n
m (H₂) = 1 г\моль ×2 моль= 2 грамма
9,5 л
Объяснение:
m(чистого Ca) = 18 г (1 - 0,02) = 17,64 г
n(Ca) = 17,64 г / 40 г/моль = 0,441 моль
Реакция с серной кислотой:
Ca + H₂SO₄ = CaSO₄ + H₂
n(прореаг H₂SO₄) = 0,441 моль
Сделаем вывод об избытке/недостатке серной кислоты:
m(H₂SO₄) = 80 г * 0,4 = 32 г
n(H₂SO₄) = 32 г / 98 г/моль = 0,327 моль
Следовательно, кислота в недостатке и n(прореаг с H₂SO₄ Ca) = 0,327 моль
Оставшийся кальций реагирует с водой:
Ca + 2H₂O = Ca(OH)₂ + H₂
Но мы видим, что в любом случае n(H₂) = n(Ca) = 0,441 моль
V(H₂) = 0,441 моль * 22,4 л/моль = 9,88 л
Но это лишь теоретический выход. Практический выход составляет 96%:
V(практический выход H₂) = 9,88 л * 0,96 ≅ 9,5 л