6) W = m / mр-ра * 100% = (0,01 моль * 187 г/моль) / 100,439г. * 100% = 1,86%;
7) W = m / mр-ра * 100% = (0,0067 моль
* 30 г/моль) / 100,439г. * 100% = 0,2%;
8) W = m / mр-ра * 100% = (0,0132 моль
*18 г/моль) / 100,439г. * 100% = 0,23%. А значит, примерно 97% - 98% массы азотной кислоты не вступило в реакцию!
ответ: W = 1,86%; W = 0,2%;
W = 0,23%. Всё!
------------------------------------------------------------------------------------------------- Есть вопросы? Задавай Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."
Задача на избыток и недостаток! Не очень сложная! Главная суть - это расчёт по недостатку, смотри:
Дано:
m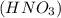 = 100г.
= 100г.
W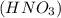 = 26%
= 26%
m(Cu) = 0,64г.
Найти:
W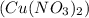 - ?
- ?
W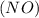 - ?
- ?
W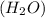 - ?
- ?
Поскольку концентрация кислоты составляет 26%, значит она разбавленная. Медь - не очень активный металл, поэтому азот восстановится до +4, т.е:
1) По уравнению, рассчитаем количество 1 моля вещества азотной кислоты:
n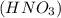 = mчист.в-ва
= mчист.в-ва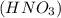 / M
/ M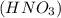 / 8 =
/ 8 =
= 100г. * 0,26 / 63 г/моль / 8 = 0,0515 моль;
2) По уравнению, рассчитаем количество 1 моля вещества меди: n(Cu) = m(Cu) / M (Cu) / 3 = 0,64г. / 63 г/моль / 3 = 0,0033 моль;
3) Значит n(Cu) - недостаток, поэтому ведём расчёты по нему. Значит, количество вещества 1 моля любого вещества в данной реакции равна 0,0033 моль.
4) По уравнению реакции: n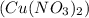 = 0,0033 моль * 3 = 0,01 моль;
= 0,0033 моль * 3 = 0,01 моль;
n(NO) = 0,0033 моль * 2 = 0,0067 моль; n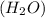 = 0,0033 моль * 4 =
= 0,0033 моль * 4 =
= 0,0132 моль;
5) mвсегор-ра = mр-ра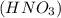 + m(Cu) - m(NO) (вычитаем выделившийся газ - оксид азота(II) = 100г. + 0,64г. - (0,0067 моль * 30 г/моль) = = 100,439г.;
+ m(Cu) - m(NO) (вычитаем выделившийся газ - оксид азота(II) = 100г. + 0,64г. - (0,0067 моль * 30 г/моль) = = 100,439г.;
6) W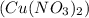 = m
= m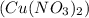 / mр-ра * 100% = (0,01 моль * 187 г/моль) / 100,439г. * 100% = 1,86%;
/ mр-ра * 100% = (0,01 моль * 187 г/моль) / 100,439г. * 100% = 1,86%;
7) W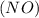 = m
= m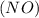 / mр-ра * 100% = (0,0067 моль
/ mр-ра * 100% = (0,0067 моль
* 30 г/моль) / 100,439г. * 100% = 0,2%;
8) W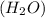 = m
= m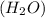 / mр-ра * 100% = (0,0132 моль
/ mр-ра * 100% = (0,0132 моль
*18 г/моль) / 100,439г. * 100% = 0,23%. А значит, примерно 97% - 98% массы азотной кислоты не вступило в реакцию!
ответ: W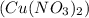 = 1,86%; W
= 1,86%; W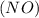 = 0,2%;
= 0,2%;
W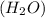 = 0,23%. Всё!
= 0,23%. Всё!
-------------------------------------------------------------------------------------------------
Есть вопросы? Задавай Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."
Пусть органическое соединение имеет состав CxHyOzNu.
M(CxHyOzNu)=DN2(CxHyOzNu)*M(N2)=1,607*28г/моль=45г/моль
1)Количество элементов,входящих в состав вещества
а)n(CO2)=V/VM=0,448л/(22,4л/моль)=0,02моль
С-->CO2
1 моль 1 моль
n©=n(CO2)=0,02 моль
m©=0,02моль*12г/моль=0,24г
б)n(N2)=0,112л/(22,4л/моль)=5ммоль
2N-->N2
2 моль 1 моль
n(N)=2n(N2)=0,01моль
m(N)=0,01моль*14г/моль=0,14г
в)n(H2O)=0,63г/(18г/моль)=0,035моль
2H-->H2
2 моль 1 моль
n(H)=2n(H2)=0,07моль
m(H)=0,07моль*1г/моль=0,07г
г)Т.к. m(N)+m(H)+m©=m(CxHyOzNu),то формулу органического вещества можно представить в виде CxHyNu
2)Определение формулы вещества
x:y:u=n©:n(H):n(N)
x:y:u=0,02:0,07:0,01;
x:y:u=2:7:1
Простейшая формула вещества-C2H7N
Mпрост.=Mист.
ответ:C2H7N