РЕШИТЬ
Периодический закон. Строение атома . Химическая связь.
2 вариант .
1.Дать характеристику атома магния по таблице
2.По электронной формуле атома определить элемент ,записать формулу его высшего оксида, определить его характер .Записать уравнения химических реакций ,характеризующих его свойства
……..2S22P.2
3.Определить тип связи и тип решетки в веществах :
Н2S , P , BаО, N2.
4.Записать электронные и структурные формулы веществ Hl , H2, KBr.
5.Определить степень окисления элементов :
Na3 PO4 , K2 O , H2SO 4 .
6.Записать уравнение реакции натрия с серой и составить к нему электронный баланс .
7.Какой объём водорода выделиться при взаимодействии 80 г кальция с серной кислотой .
1. a) CaO,
в)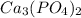
б) HCl
г)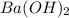
д)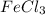
2. Азотная кислота, оксид алюминия (3), гидроксид кальция, сульфат магния, ортофосфорная кислота
3.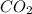 , MgO,
, MgO, 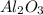 ,
, 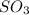 ,
, 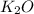
4. В первом +3(промежуточная), во втором -3(низшая), в третьем +5(высшая), в четвертом +2(промежуточная).
5. Решим простую математическую задачу: 200л(полный объем воздуха) * 21%(о,21) = 42 л кислорода
6. Найдём массу1 сахара = о,2 * 80 = 16 кг
найдем массу сахара2 = 16 + 15 = 31 кг
найдем массу раствора2 = 80 + 15 = 95 кг
И новая массовая доля равна: 31/95 * 100% (масса вещества/массу раствора) = 32,63 % или 33%