С ХИМИЕЙ!
7. Сложное вещество, при диссоциации которого образуется один катион и два сложных аниона. Укажите названия видов связи между всеми частицами вещества.
8. Бинарное соединение натрия, содержащее ковалентную неполярную и ионные связи. Укажите названия видов связи между всеми частицами вещества.
9. Соль, образованная катионом с зарядом 2+ и анионом в котором количество химических связей (валентность) не совпадает с числом отданных электронов (степенью окисления). Укажите названия видов связи между всеми частицами вещества.
ЧАСТЬ А.
1. Распределение электронов по энергетическим уровням в атоме кислорода.
А. 2ē, 6ē
*Так как кислород находится во втором периоде, он имеет 2 энергетических уровня. В тоже время кислород расположен в VIA группе, значит на внешнем энергетическом уровне у него находится 6 электронов.
2. Формула вещества с ковалентной полярной связью:
В. Н2О
*Ионная связь возникает между атомами металла и неметалла, из данных вариантов ионной связью обладают соединения CaO и NaCl.
Ковалентной полярной связи присуща связь между атомами двух неметаллов, ею обладает соединение H2O.
Ковалентная неполярная связь образуется в простых веществах, она характерна для соединения О2.
3. Ряд формул веществ, в котором степень окисления серы уменьшается:
В. SO2—S—H2S
*S(+4)O2—S(0)—H2S(-2)
4. Неметаллические свойства в ряду химических элементов O-S-Se-As:
В.Ослабевают
*Чем дальше от самого элекроотрицательного элемента - фтора, тем менее выражены неметаллические и окислительные свойства.
По периодической таблице Менделеева неметаллических свойства ослабевают сверху вниз, справа налево.
5. Сумма всех коэффициентов в уравнении реакции, схема которой H2S+O2 -> SO2 + H2O
В. 9
*2H2S + 3O2 -> 2SO2 + 2H2O
2+3+2+2=9
6. Уравнение реакции, в котором элемент сера является восстановителем:
Б. S +O2 -> SO2
*S(0) + O2(0) -> S(+4)O2(-2)
S(0)--(-4ē)-->S(+4) | 4 | ×1
- восстановитель(отдает электроны), процесс окисления
O2(0)--(+4ē)-->2O(-2)|4|×1
- окислитель(получает электроны), процесс восстановления.
7. Свойство, характерное для серы: В. Твердое вещество желтого цвета
8. Массовая доля кислорода наименьшая в соединении с формулой:
А. K2O
*Mr(K2O)=39×2+16=94
w(O)=(16/94)×100%=17%
Mr(H2O)=1×2+16=18
w(O)=(16/18)×100%=88.9%
Mr(Li2O)=7×2+16=30
w(O)=(16/30)×100%=53.3%
Mr(Na2O)=23×2+16=62
w(O)=(16/62)×100%=25.8%
9. Оксид серы(6) реагирует с веществом, формула которого:
Б. NaOH
*SO3 - оксид серы(6)
SO3 + 2NaOH -> Na2SO4 + H2O
Признаком прохождения реакции является образование малодиссоциирующего вещества - воды.
10. Сокращенное ионное уравнение реакции, соответствующее молекулярному H2SO4 + Zn = ZnSO4 +H2⬆️
В. 2H(+) + Zn = Zn(+2) + H2⬆️
*Полное ионное:
2H(+)+SO4(-2) + Zn -> Zn(+2)+SO4(-2) + H2⬆️
После сокращения сульфат-ионов получаем сокращенное ионное уравнение реакции.
ЧАСТЬ Б.
11. SO2—H2SO3—Na2SO3—MgSO3
*Молекулярное:
SO2 + H2O <-> H2SO3
Полное ионное:
SO2 + H2O <-> 2H(+)+SO3(-2)
Сокращенное ионное будет тем же, что полное.
Молекулярное:
H2SO3 + 2NaOH -> Na2SO3 + 2H2O
Полное ионное:
2Н(+)+SO3(-2) + 2Na(+)+2OH(-) -> 2Na(+)+SO3(-2) + 2H2O
Сокращенное ионное:
H(+) + OH(-) -> H2O
Молекулярное:
Na2SO3 + MgCl2 -> MgSO3⬇️ + 2NaCl
Полное ионное:
2Na(+)+SO3(-2) + Mg(+2)+2Cl(-) -> MgSO3⬇️ + 2Na(+)+2Cl(-)
Сокращенное ионное:
SO3(-2) + Mg(+2) -> MgSO3⬇️
12.
*Cu + 2H2SO4(конц) -> CuSO4 + SO2 + 2H2O
С расставленными степенями окисления:
Cu(0) + 2H2(+)S(+6)O4(-2) -> Cu(+2)S(+6)O4(-2) + S(+4)O2(-2) + 2H2(+)O(-2)
Cu(0)--(-2ē)-->Cu(+2)2 | ×1
- восстановитель(отдает электроны), процесс окисления
S(+6)--(+2ē)-->S(+4) | 2 | ×1
- окислитель(получает электроны), процесс восстановления.
13. Газометр служит для сбора и хранения газообразных веществ, таких как кислород и т.д., грубого измерения их объемов.
14. С какого катиона можно распознать сульфат-ион?
*Для распознавания сульфат-иона(SO4(-2)) можно использовать катион бария(Ba(+2)).
Например, имеется растворы сульфата натрия и хлорида бария. Запишем уравнение реакции между ними в молекулярном виде:
Na2SO4 + BaCl2 -> BaSO4⬇️ + 2NaCl
В полном ионном:
2Na(+)+SO4(-2) + Ba(+2)+2Cl(-) -> BaSO4⬇️ + 2Na(+)+2Cl(-)
В сокращенном ионном:
SO4(-2) + Ba(+2) -> BaSO4⬇️
15. Дано:
Q1=572 кДж
Q2=1144 кДж
V(H2)-?
1 Уравнение реакции:
2H2(г) + O2(г) -> 2Н2О(ж) + 572 кДж
2 По уравнению реакции видно, что из двух моль водорода образуется 572 кДж энергии. Необходимо найти количество, из которого образуется 1144 кДж.
Составим пропорцию:
2/x=572/1144
x=(2×1144)/572
x=4 моль
3 Теперь найдем объем водорода:
V=n×Vm
Vm=22.4 л/моль
V(H2)=4×22.4=89.6 л
ответ: 89.6 л
1.
А.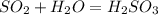
Б.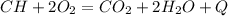
В.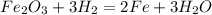
1.
А.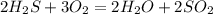
Б.
В.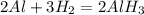
2.
mH2O = 35г
mсоли = 10г
mраствора = mсоли+mводы = 35г+10г = 45г
w = mсоли/mр-ра = 10г/45г*100% = 22,2%
2.
mр-ра = 300г
wсоли = 0,05
mсоли = w*mр-ра = 0,05*300г = 15г
mводы = mр-ра - mсоли = 300-15 = 285г
3.
C -> XH4 -> CO2 -> H2CO3
1. C + 2H2 = CH4 - соединение, обр. метан
2. CH4 + 2O2 = CO2 + 2H2O - разложение, с образованием углекислого газа и воды.
3. CO2 + H2O = H2CO3 - соединение, обр. уголная кислота
3.
Al -> Al2O3 -> Al -> Al(OH)3
1. 4Al + 3O2 = 2Al2O3 - соединение, обр. оксид алюминия.
2. 2Al2O3 --эл. ток--> 4Al + 3O2 - разложение, обр. алюминий и кислород
3. 2Al + 6H2O = 2Al(OH)3 + 3H2 - замещение, обр. гидроксид алюминия и водород.