с задачами по химии! Очень нужно! 1.Определите молярность 20%-ного раствора, содержащего фосфорной кислоты(Н3РО4) (р=1,1 г/мл), объемом 550мл.
2.Вычислите массовую долю растворенного вещества в 0,5 м растворе хлорида кальция(СаСL2) (p r=1,02 г/мл), объемом 1л.
3. Сколько граммов вещества нужно взять для приготовления 2кг 10% раствора сульфата цинка(ZnSO4).
Mr (CaCO3) = 40 + 12 + 16 ∙ 3 = 100
Mr ((CuOH)2CO3) = (64 + 16 +1)∙2 + 12 + 16∙3 = 222
Mr (С12H22O11) = 12 ∙ 12 + 1∙22 + 16∙11 = 342
Mr (FeSO4*7H2O) = 56 + 32 + 16∙4 + 7(1∙2+16) = 278
Задание 2:
Дано:
n(С12H22O11) = 2,5 моль
Найти: m (С12H22O11), N(С)
Решение:
M (С12H22O11) = 342 г\моль
m(С12H22O11) = n ∙ M = 2,5 моль ∙ 342 г\моль = 855 г
n(С) = 12 ∙ n(H3PO4) = 12 ∙ 2,5 = 30 моль
N(С) = Na ∙ n = 6,023 ∙ 10 [23] ∙ 30 = 1,8 ∙ 10[25] атомов
ответ: m (С12H22O11) = 855 г, N(С) = 1,8 ∙ 10[25] атомов
Задание 3:
Дано:
m (H3PO4) = 19,6 г
Найти: N(O)
Решение:
M (Н3PO4) = 1∙3 + 31 + 16∙4 = 98 г\моль
n(H3PO4) = m\M = 19,6 г\98 г\моль = 0,2 моль
n(O) = 4 ∙ n(H3PO4) = 4 ∙ 0,2 = 0,8 моль
N(O) = Na ∙ n = 6,023 ∙ 10 [23] ∙ 0,8 = 4,8 ∙ 10[23] атомов
ответ: N(O) = 4,8 ∙ 10[23] атомов
4 задание:
Решение:
В 1 моле серной кислоты содержится 4 моль атомов кислорода
Найдем число молей атомов кислорода в серной кислоте количеством вещества 1 моль: n(O) = 4 ∙ n(H2SO4) = 4 ∙ 1 = 4 моль
В 1 моле воды содержится 1 моль атомов кислорода
вычислим сколько молей будут составлять 4 моля атомов кислорода:
n(H2O) = n(O)\1 = 4\1 = 4 моль
ответ: число молей кислорода в 1 моле серной кислоты будут соответствовать 4 молям воды
№1:
а -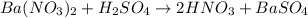
б -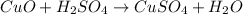
в -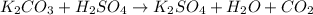
г -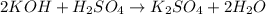
Про тесения реакций - извини, не очень понял, что требуется?
№3
Качественная реакция на сульфат - анион есть реакция с катионами бария:
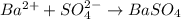 - выпадает белый осадок сульфата бария, такая реакция есть в задании №1 под пунктом - а
- выпадает белый осадок сульфата бария, такая реакция есть в задании №1 под пунктом - а
№4 В обе пробирки добавить несколько мл гидроксида бария. В пробирке с соляной кислотой пройдет обычная нейтрализация, видимых изменений не наблюдается, а в пробирке с серной кислотой выпадет белый осадок сульфата бария(ионные уравнения приведены выше)