Ть 1. позначте формулу оцтової кислоти: а.с2н5он; б. нсоон; в.сн3соон; г. с17н35соон. 2. загальна формула насичених одноатомних спиртів: а. сп(н2о)m; б. r1cооr2; в. сн3соон; г. спн2п +1он. 3. функціональна группа карбонових кислот: 4. жири – це органічні речовини, що належать до класу: а. спиртів; б. естерів; в. карбонових кислот; г. вуглеводів. 5. оцтова кислота змінює колір лакмусу на: а. фіолетовий; б. червоний ; в. малиновий; г. синій. 6. гексаналь належить до: а. спиртів; б. карбонових кислот; в. альдегідів; г. жирів. завдання 7 – 9 можуть мати дві і більше правильні відповіді. 7. (0,5 б.) укажіть властивості етанолу, що спричиняють його застосування у фармацевтичній промисловості: а) чудовий розчинник і антисептик; б) має слабку наркотичну дію; в) добре розчиняється у воді. 8. (0,5 б.) .гліцерин застосовують для добування: а) динаміту; б) ліків; в) антифризів. 9. (1б.) позначте речовини, з якими може реагувати етиловий спирт: а. na; б. сн3соон; в. сасо3; г. нcl. 10.(2б.)закінчити рівняння реакцій: а. сн3соон + nа2со3 → ; в. с7н15он + о2 →; б. сн3 – соон + к → ; г. с4н9он + hcl →
Все химические элементы можно охарактеризовать в зависимости от строения их атомов, а также по их положению в Периодической системе Д.И. Менделеева. Обычно характеристику химического элемента дают по следующему плану:
указывают символ химического элемента, а также его название;
исходя из положения элемента в Периодической системе Д.И. Менделеева указывают его порядковый, номер периода и группы (тип подгруппы), в которых находится элемент;
исходя из строения атома указывают заряд ядра, массовое число, число электронов, протонов и нейтронов в атоме;
записывают электронную конфигурацию и указывают валентные электроны;
зарисовывают электронно-графические формулы для валентных электронов в основном и возбужденном (если оно возможно) состояниях;
указывают семейство элемента, а также его тип (металл или неметалл);
указывают формулы высших оксидов и гидроксидов с кратким описанием их свойств;
указывают значения минимальной и максимальной степеней окисления химического элемента.
0 0 +1 -1
1)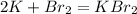
0 +1
K -1e = K |2|восстановитель(окисление)
0 -1
Br2 + 2e = 2Br |1|окислитель(восстановление)
0 0 +2 -3
2)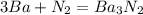
0 +2
Ba - 2e = Ba |3|восстановитель(окисление)
0 -3
N2 + 6e = 2N |1|окислитель(восстановление)
0 +1 +2 0
3)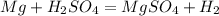
0 +2
Mg -2e = Mg |1|восстановитель(окисление)
+1 0
2H +2e = H2 |1|окислитель(восстановление)
0 +1 +1 0
4)
0 +1
Li - 1e = Li |2|восстановитель(окисление)
+1 0
2H + 2e = H2 |1|окислитель(восстановление)