Тематичне оцінювання № 1 за темою «розчини» завдання 1- 5 мають завданні лише одну правильну відповідь. 1. в якій із зазначених груп йонів знаходяться лише аніони: а) к + , сl¯, mg 2+ , h + ; б) он¯, so 4 2 ¯, cl¯, po 4 3 ¯; в) аl 3+ , na + , ca 2+ , zn 2+ . 2. яка з речовин у водному розчині дисоціює з утворенням йону мg 2+ а) mgcl 2 ; б) mgco 3 ; в) mgo. 3. серед запропонованих речовин виберіть формулу електроліту: а) na 2 o; б) naoh; в) h 2 . 4. вкажіть формулу слабкого електроліту: а) н 2 со 3 ; б) кон; в) nacl. 5. вкажіть йон, який завжди утворюється при дисоціації кислот: а) гідроген-йон; б) гідроксид-йон; в) йон металу. у завданнях 6–8 оберіть всі правильні відповіді 6. позначте символ та одиниці вимірювання масової частки: а) %; б) г; в) ω; г) α. 7. в результаті дисоціації натрій сульфату утворились йони: а) н + ; б) na + ; в) so 4 2- ; г) он - . 8. які із зазначених нижче пар йонів не можуть одночасно перебувати в розчині? чому? а) zn 2+ і сl - ; б) сu 2+ і ро 4 3- ; в) мg 2+ і он - ; г) мg 2+ і nо 3 - завдання 9 має на меті встановити відповідність. до кожного рядка, позначеного буквою, доберіть відповідник, позначений цифрою. 9. установіть відповідність між умовами перебігу реакцій йонного обміну до кінця та реагентами. умови перебігу реакцій реагенти а. випадання осаду 1. mgso 4 + koh → б. виділення газу і води 2. al 2 (so 4 ) 3 + nacl → b. утворення води 3. к 2 со 3 + нсl → 4. lioh + h 2 so 4 → напишіть молекулярні та йонні рівняння. завдання 10 – 13 передбачають певні обчислення або письмове пояснення. 10. складіть два молекулярних рівняння реакцій між речовинами, які у розчинах взаємодіють за такою схемою: fe 2+ + 2oh - → fe(oh) 2 11. електроліт має ступінь дисоціації 20%. скільки молекул розпалося на йони з кожних 200 молекул? 12. обчислити масову частку речовини в розчині, якщо в 200 г води розчинили 10 г речовини. 13. запропонуйте, як насичений солі розчин зробити ненасиченим.
Объяснение:
1) Б
2) А
3) Б
4) А
5) А
6) В, А
7) Б, В
8) Б - выпадает осадок, в - аналогично
9) А1, Б3, В4
10) FeCl2+2NaOH=2NaCl+Fe(OH)2↓
FeSO4+2KOH=K2SO4+Fe(OH)2↓
11) 200*0,2=40
12) масса раствора 200+10=210г
w=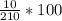 =4,76%
=4,76%
13) воды добавьте или подогрейте