Укажите распределение электронов по энергетическому уровню, соответствующее атому неметалла 1) 2e,8e,8e,1e 2) 2e,8e,1e 3)2e,8e,7e 4)2e,8e,2e 2)Какие из двух оксидов относятся к солеобразующим 1)N2O и CO2 2)N2O5 и CO 3)NO и CO 4)N2O3 и CO2
6- Ca и Ba - элементы второй группы главной подгруппы. В периодической системе сверху вниз увеличиваются металлические свойства. Это объясняется тем, что сверху вниз увеличивается число энергетических уровней, следовательно увеличивается радиус атома. Чем больше радиус атома, тем меньше энергия ионизации. Энергия ионизации (энергия, которую необходимо затратить для отрыва e от атома и превратить его в ион) - уменьшается, а чем меньше энергия ионизации, тем легче оторвать электрон от атома, тем сильнее металлические свойства.
ответ: Ba (Барий)
7- P и Cl - элементы третьего малого периода. В периодической системе слева направо увеличиваются неметаллические свойства. Это объясняется тем, что слева направо уменьшается радиус атома. Чем меньше радиус атома, тем больше энергия сродства к электронам (характеристика неметалличности). Это энергия, которая выделяется при присоединении к атому электронов. чем больше энергия сродства к электронам, тем сильнее выражены неметаллические свойства.
6- Ca и Ba - элементы второй группы главной подгруппы. В периодической системе сверху вниз увеличиваются металлические свойства. Это объясняется тем, что сверху вниз увеличивается число энергетических уровней, следовательно увеличивается радиус атома. Чем больше радиус атома, тем меньше энергия ионизации. Энергия ионизации (энергия, которую необходимо затратить для отрыва e от атома и превратить его в ион) - уменьшается, а чем меньше энергия ионизации, тем легче оторвать электрон от атома, тем сильнее металлические свойства.
ответ: Ba (Барий)
7- P и Cl - элементы третьего малого периода. В периодической системе слева направо увеличиваются неметаллические свойства. Это объясняется тем, что слева направо уменьшается радиус атома. Чем меньше радиус атома, тем больше энергия сродства к электронам (характеристика неметалличности). Это энергия, которая выделяется при присоединении к атому электронов. чем больше энергия сродства к электронам, тем сильнее выражены неметаллические свойства.
ответ: Cl (Хлор)
8-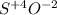
Fe⁺²O
1.Определить вид химической связи для следующих веществ:
О2 - ковалентная неполярная
Ва - металлическая
КСl ионная
H2О. - ковалентная полярная.
2.Назовите химические элементы, определите заряды ядер, тип элемента (металл или неметалл), к какому семейству (s, p, d, f) принадлежат эти элементы:
а) 1s22s22p63s2 - магний, заряд ядра +12, металл, s - элемент
в) 1s22s22p3 - азот, заряд ядра +7, неметалл, р-элемент
б) 1s22s22p4 - сера, заряд ядра +16, неметалл, р-элемент
г) 1s22s22p63s23p64s2 - кальций, заряд ядра +20, металл, s - элемент,
д) 1s22s22p63s1 - натрий, заряд ядра +11, металл, s - элемент,
е) 1s22s22p3 (такой же как и под буквой в)
3. а) Расположите химические элементы в порядке возрастания
металлических свойств: Ge, Pb, Si.
Si → Ge → Pb
б) Расположите химические элементы в порядке возрастания
неметаллических свойств: S, Al, P.
Al → Р → S
4. Определите число протонов, нейтронов и электронов для изотопов фосфора: 30Р 31Р и неона 20Ne 21Ne.
³⁰Р - 15 протонов, 15 нейтронов, 15 электронов
³¹Р - 5 протонов, 156 нейтронов, 15 электронов
²⁰Ne - 10 протонов, 10 нейтронов, 150 электронов
²¹Ne - 10 протонов, 11 нейтронов, 150 электронов
5. Назовите химические элементы, а также определите заряды ядер
этих атомов, зная распределение электронов по энергетическим
уровням:
2, 8, 7 - хлор, заряд ядра +17, неметалл
2, 6 - - кислород , заряд ядра +8, неметалл
2, 8, 1 - натрий, заряд ядра +11, металл