Уравнения а4 реакции. при
нормальных условиях по уравнению реакции.
уровень мыслительных
знание и понимание
авыков применение. время выполнения 35 мин
не 11
. в-1
no 1 заполни таблицу
вычисление
объем
число молекул
| масса
количество в-ва
1 моль cl2
3 моль сі,
200 гci,
i
44,8л
в-2
no 1 заполни таблицу
вычисление
масса
объем
| количество в-ва | число молекул
1 моль n2
3 моль n.
200 г n2
| 44,8л n2
no2
в-1вычислить массу и количество вещества углекислого газа, образующегося при сжигании 20 к
угля.
в-2 вычислить количество вещества и массу оксида серы(4), образующегося при сжигании 20 г.
Дано:
m(C₁₂H₂₂O₁₁) = 342 гр
Найти:
N(AТФ) - ?
1) Сахароза – дисахарид и состоит из α-D-глюкозы и β-D-фруктозы, их энергетическая ценность при окислении одинакова.
C₁₂H₂₂O₁₁ + H₂O (H⁺ , t°C)→ C₆H₁₂O₆ + C₆H₁₂O₆
Сахароза α-D-глюкоза β-D-фруктоза
2) Для начала мы найдем молекулярную массу сахарозы, а потом находим количества молекул у сахарозы а потом у глюкозы:
M(C₁₂H₂₂O₁₁) = 12×12 + 1×22 + 16×11 = 144 + 22 + 176 = 342 гр/моль
n(C₁₂H₂₂O₁₁) = m(C₁₂H₂₂O₁₁)/M(C₁₂H₂₂O₁₁) = 342 гр / 342 гр/моль = 1 моль ⇒ n(C₆H₁₂O₆) = n(C₁₂H₂₂O₁₁) = 1 моль
3) Теперь находим количества вещества у сахарозы:
N(C₁₂H₂₂O₁₁) = n(C₁₂H₂₂O₁₁)×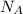 = 1 моль × 6,02×10²³ (моль)⁻¹ = 6,02×10²³ молекул
= 1 моль × 6,02×10²³ (моль)⁻¹ = 6,02×10²³ молекул
4) Теперь найдем сколько молекул АТФ образовалось в результате анаэробного и аэробного условия, зная что в результате анаэробного условия образуется 3 молекулы АТФ, а в результате аэробного условия 38 молекул (в расчёте на 1 молекулу глюкозы):
N(АТФ) = n(АТФ)×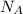 = 3 моль × 6,02×10²³ (моль)⁻¹ = 18,06×10²³ молекул - при анаэробном условий.
= 3 моль × 6,02×10²³ (моль)⁻¹ = 18,06×10²³ молекул - при анаэробном условий.
N(АТФ) = n(АТФ)×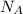 = 38 моль × 6,02×10²³ (моль)⁻¹ = 228,76×10²³ молекул - при аэробном условий.
= 38 моль × 6,02×10²³ (моль)⁻¹ = 228,76×10²³ молекул - при аэробном условий.
ответ: N(АТФ) = 18,06×10²³ молекул - при анаэробном условий.
N(АТФ) = 228,76×10²³ молекул - при аэробном условий.
Решено от :
1.Дождевая вода в отличие от ключевой не содержит растворенных солей. Поэтому ключевая иода более жесткая Жесткая вода - вода содержащая в себе значительное количество растворённых солей кальция и магния Виды жесткости: временная, постоянная и обшая.
2. Кислородсодержащие кислоты (оксокислоты) получают взаимодействие кислотных оксидов с водой (реакция соединения). Однако очень немногие кислотные оксиды не взаимодействуют с водой. Этим методом не получают труднорастворимые оксокислоты, например, H2SiO3. Кислотный оксид + H2O = Оксокислота. SO3 + H2O = H2SO4 P2O5 + 3H2O = 2H3PO4. Получение кислородсодержащих кислот взаимодействием кислотного оксида с водой. Общий получения кислот. Большинство кислот можно получить действием на соль сильной или менее летучей кислоты (реакция обмена