Решение: 1. Реакция ионного обмена. Очевидно, что в результате выделиться сульфат бария (это и есть осадок, от которого отделили раствор) и хлорид меди. 2. На электродах происходит электролиз хлорида меди. На катоде будет восстанавливаться медь. 3. При реакции меди с концентрированной серной кислотой будет образовываться сульфат меди, диоксид серы (он же и есть тот самый газ в условии) и вода. 4. Здесь протекает реакция окислительно-восстановительная. Сульфат калия здесь получился потому, что в результате реакции на самом деле будет оксид серы (VI), но так, как наша среда щелочная (а щелочь, увы, там ни с чем, кроме получившегося оксида, не будет реагировать), там будет образовываться сульфат калия.
Для выражения частиц содержащихся, в определенной массе или объеме вещества, введено понятие количества вещества. Единицей количества вещества является моль. 1 моль-такое количество вещества, в котором содержиться 6,02* 10 в 23 степени частиц(атомов, молекул. ионов)
Na - постоянное авогадро равно 6,02*10 в 23 степени частиц.
Ню -число моль показывет взаимодействие числа моль и кол-ва частиц
Молярная масса численно равна относительной молярной массе
1. Реакция ионного обмена. Очевидно, что в результате выделиться сульфат бария (это и есть осадок, от которого отделили раствор) и хлорид меди.
2. На электродах происходит электролиз хлорида меди. На катоде будет восстанавливаться медь.
3. При реакции меди с концентрированной серной кислотой будет образовываться сульфат меди, диоксид серы (он же и есть тот самый газ в условии) и вода.
4. Здесь протекает реакция окислительно-восстановительная.
Сульфат калия здесь получился потому, что в результате реакции на самом деле будет оксид серы (VI), но так, как наша среда щелочная (а щелочь, увы, там ни с чем, кроме получившегося оксида, не будет реагировать), там будет образовываться сульфат калия.
Для выражения частиц содержащихся, в определенной массе или объеме вещества, введено понятие количества вещества. Единицей количества вещества является моль. 1 моль-такое количество вещества, в котором содержиться 6,02* 10 в 23 степени частиц(атомов, молекул. ионов)
Na - постоянное авогадро равно 6,02*10 в 23 степени частиц.
Ню -число моль показывет взаимодействие числа моль и кол-ва частиц
Молярная масса численно равна относительной молярной массе
Пример:
Массу угарного газа возьмем 28 г
Ню(CO)=m/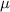 =28/28=1 моль
=28/28=1 моль