Задание 2. Напишите структурные формулы всех возможных изомеров веществ: пентана, дихлорметана СН2С12, в соответствии с ними сделайте шаровидные модели изомеров на примере бутана и изобутана.
1. Валентность есть изменяемая и неизменная. Ищем элемент, у которого неизменная валентность и спрашиваем у таблицы Менделеева или вспоминаем. У кислорода(О) валентность 2, у водорода(Н) - 1, у магния(Mg) - 2. Атом электронейтрален, поэтому сумма зарядов всегда равна нулю. Считаем с учетом индексов. 2. Находим молярную массу оксида меди(2) (M(CuO)) как сумму относительных атомных масс элементов, входящих в оксид( см. в таблице Менделеева). Затем по формуле n=m/M находим кол-во вещества(n). 3. По закону сохранения масс сравниваем кол-во атомов каждого элемента справа и слева и домножаем, чтобы это кол-во уравнять. 4. Про нахождение молярной массы я писала выше, а массовая доля находится по вот такой формуле: Ar(элемента с учетом индексов)/М(вещества) 5. Уравнение реакции: Mg + 2HCl = MgCl2 + H2 Находим кол-во вещества магния и смотрим на уравнение. Коэффициенты одинаковые, значит, кол-ва веществ одинаковы тоже. По формуле V = nVм, где Vм - молярный обьем, который равен 22,4 л, находим обьем водорода. Вопросы есть?
Начнем - с.
Гидролиз пойдет по аниону -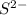
1 - ступень:
Молекулярный Вид: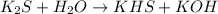
2 - ступень:
Молекулярный вид: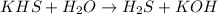
гидролиз пойдет по катиону -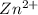
1 - ступень:
МВ: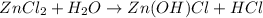
2 - ступень:
МВ: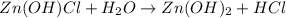
1 - ступень:
МВ: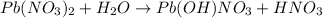
2 - ступень:
МВ: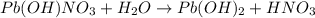
1 - ступень:
МВ: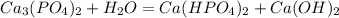
2 - ступень:
МВ: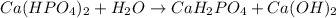
3 - ступень:
МВ: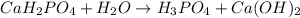 среда щелочная, лакмус синий
среда щелочная, лакмус синий
МВ: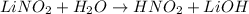
1 - ступень:
МВ: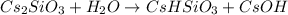
2 ступень:
МВ: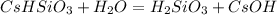
1 - ступень:
МВ: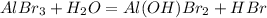
2 - ступень:
МВ: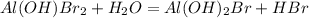
3 - ступень
МВ: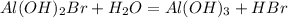
2. Находим молярную массу оксида меди(2) (M(CuO)) как сумму относительных атомных масс элементов, входящих в оксид( см. в таблице Менделеева). Затем по формуле n=m/M находим кол-во вещества(n).
3. По закону сохранения масс сравниваем кол-во атомов каждого элемента справа и слева и домножаем, чтобы это кол-во уравнять.
4. Про нахождение молярной массы я писала выше, а массовая доля находится по вот такой формуле: Ar(элемента с учетом индексов)/М(вещества)
5. Уравнение реакции: Mg + 2HCl = MgCl2 + H2
Находим кол-во вещества магния и смотрим на уравнение. Коэффициенты одинаковые, значит, кол-ва веществ одинаковы тоже. По формуле V = nVм, где Vм - молярный обьем, который равен 22,4 л, находим обьем водорода.
Вопросы есть?