ответ: 80 грамм
Объяснение:
2NaOH + CO2 = Na2CO3 + H2O
Если условия нормальные, то 1 моль газа занимает 22.4 литра
1 моль - 22.4 литра
х моль - 4.48 литра
х = 4.48 / 22.4 = 0.2 моль
Посмотрим в реакцию. Если СО2 - 0.2 моля, то сколько молей нужно NaOH. Очевидно, в два раза больше.
Найдем массу едкого натра
0.4 моля * (23+16+1) г/моль = 16 грамм
Найдем массу раствора
16 грамм - 20%
х грамм - 100%
х = 8*100/20 = 80 г
модератору за указание на арифметические ошибки, но можно было и не так эмоционально )))
х г 2,24 л
1.
65 г 22,4 л
1) Так как медь с соляной кислотой не взаимодействует,а будет взаимодействовать цинк,вот его-то массу и найдем по объему выделившегося водорода:
при взаимодействии 65 г цинка выделяется 22,4 л, а
при -- // -- // -- х г__________________2,24 л, откуда
х=65*2,24/22,4=6,5 г
2) Если эту массу отнести к массе всего образца,то узнаем массовую долю цинка в сплаве:
w(Zn)=m(Zn)/m(сплава)=6,5/25,8=0,25 или 25%
3) А на медь приходится: 100% - 25% = 75%
84 г х г
2.
261 г 165 г
при взаимодействии 261 г оксида восстанавливается 165 г марганца, а
при -- // -- // -- 84 г_________________________х г, откуда
х=84*165/261= 53 г
ответ: 80 грамм
Объяснение:
2NaOH + CO2 = Na2CO3 + H2O
Если условия нормальные, то 1 моль газа занимает 22.4 литра
1 моль - 22.4 литра
х моль - 4.48 литра
х = 4.48 / 22.4 = 0.2 моль
Посмотрим в реакцию. Если СО2 - 0.2 моля, то сколько молей нужно NaOH. Очевидно, в два раза больше.
Найдем массу едкого натра
0.4 моля * (23+16+1) г/моль = 16 грамм
Найдем массу раствора
16 грамм - 20%
х грамм - 100%
х = 8*100/20 = 80 г
модератору за указание на арифметические ошибки, но можно было и не так эмоционально )))
х г 2,24 л
1.
65 г 22,4 л
1) Так как медь с соляной кислотой не взаимодействует,а будет взаимодействовать цинк,вот его-то массу и найдем по объему выделившегося водорода:
при взаимодействии 65 г цинка выделяется 22,4 л, а
при -- // -- // -- х г__________________2,24 л, откуда
х=65*2,24/22,4=6,5 г
2) Если эту массу отнести к массе всего образца,то узнаем массовую долю цинка в сплаве:
w(Zn)=m(Zn)/m(сплава)=6,5/25,8=0,25 или 25%
3) А на медь приходится: 100% - 25% = 75%
84 г х г
2.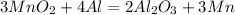
261 г 165 г
при взаимодействии 261 г оксида восстанавливается 165 г марганца, а
при -- // -- // -- 84 г_________________________х г, откуда
х=84*165/261= 53 г