Завдання 3. Учень приготував 60 г розчину з масовою часткою речовини 15%. Йому необхідно було приготувати розчин з масовою часткою речовини 12%.
Скільки грамів води треба додати до виготовленого розчину, щоб отримати
потрібний (з масовою часткою 12%)? Проведіть необхідні розрахунки,
оформіть як розрахункову задачу.
Підказка: ми маємо два розчини, записуємо формули: для першого розчину
Wi-mi речовини/m1 розчину, відповідно для другого розчину W=m2 речовини/m2 ретчину-
Для того, щоб зменшити масову частку речовини в розчині, потрібно додати
води (розчинника). Це вплине на масу розчину, вона збільшиться. Речовину в
даному випадку додавати не треба, то ті речовини = m2 речовини.
Висновки. Які уміння й навички Ви закріпили при виконанні даної роботи?
Де можть вони знадобитися?
О
а д.
УКР 20-21
UKRE 18052021
Для начала определим относительную плотность искомого вещества.
Формула для вычисления относительной плотности:
D (по водороду) =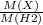 = 28 (молярная масса искомого вещества принята за Х).
= 28 (молярная масса искомого вещества принята за Х).
Тогда:
Х = 28 * M(H2) = 28 * 2 = 56 г/моль
В искомом веществе n(C) = m(CO2) : M (CO2) = 17,6 г : 44 г/моль = 0,4 моль (атомов углерода), соответственно:
m(C) = n(C) * M(C) = 0,4 моль * 12 г/моль = 4,8 г
Если все вещество весит 5,6 г, то, следовательно, масса атомов водорода:
m(H) = 5,6 г - 4,8 г = 0,8 г
поэтому представим искомую формулу углеводорода таким образом:
CxH2x
14x=56
x=4
значит, C4H8 - истинная формула вещества (бутен)
ответ: C4H8
Чтобы понять, как решаются конкретные химические уравнения (где соль реагируют с металлом), обратимся к электрохимическому ряду напряжений металлов.
Все металлы, находящиеся перед H в данном ряду (с лития Li по свинец Pb) являются активными металлами. После Н (с Sb по Au) расположены неактивные (или же малоактивные металлы).
В нашем случае реакция пойдет, если соль, включающая в себя менее активный металл прореагирует с более активным металлом, а в итоге получится соль, состоящая из более активного металла и менее активный металл. То есть:
Zn - более активный металл (обращаемся к ряду напряжений, он стоит до водорода) реагирует с солью CuSO4, где металлом является Cu, он стоит после водорода и является менее активным по сравнению с Zn соответственно. Ну и в итоге, как написано выше, более активный Zn присоединяется к кислотному остатку SO4.
Вообще, если говорить об уравнениях с солями в целом, нужно заучивать что с чем реагирует и что в итоге получается. Вот остальные реакции с солями с примерами:
1) соль + основание = основание + соль
Ba(OH)2 + Na2SO4 = 2NaOH + BaSO4 ↓ (тут элементы как бы меняются местами, сначала был гидроксид бария, а потом соль с ним, была соль с натрием, стал гидроксид с ним)
2) соль + кислота = кислота + соль
H2SO4 + BaCl2 = 2HCL + BaSO4 ↓ (тут ситуация аналогичная элементы меняются местами барий образует соль с кислотным остатком so4, а был с cl)
3) соль + кислотный оксид = кислотный оксид + соль (при t)
SiO2 + CaCO3 = CaSiO3 + CO2↑
4) соль + соль = соль + соль
AgNO3 + NaCl = AgCl ↓ + NaNO3
если что-то еще не понимаешь - спрашивай, постараюсь объяснить :)