Медь, содержащаяся в 0.1200 г сплава, переведена в раст- вор. При добавлении к этому раствору избытка йодида калия выде- лился йод, на титрование которого было затрачено 13.8 см3 раствора тиосульфата натрия с титром 0.0140 г/см3. Рассчитайте массовую долю меди в сплаве.
S - елементы:
H -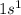
He -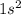
Li -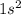
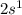
Be -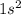
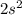
Na -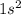
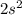
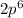
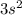
P - елементы:
B -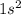
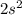
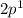
C -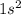
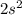
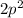
N -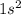
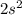
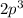
O -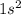
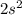
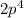
F -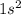
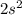
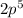
D - елементы:
Sc - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^1
Ti - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^2
V - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^3
Cr - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^1 3d^5
Mn - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^5
F - елементы:
Ce - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^10 4p^6 5s^2 4d^10 5p^6 6s^2 4f^2
Pr - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^10 4p^6 5s^2 4d^10 5p^6 6s^2 4f^3
Nd - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^10 4p^6 5s^2 4d^10 5p^6 6s^2 4f^4
Pm - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^10 4p^6 5s^2 4d^10 5p^6 6s^2 4f^5
Sm - 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^10 4p^6 5s^2 4d^10 5p^6 6s^2 4f^6
Значок ^ это показатель степени
На сегодняшний день Иссыкские курганы являются ярким примером того, как распространилось искусство звериного стиля и откуда произошло. В палеометаллическую эпоху уже были известны предметы и вещи, выполненные в зверином стиле не только на территории Центральной Азии, но и всей Евразии. В особенности, андроновцам Казахстана и Сибири были хорошо известным андроновским племенам Сибири и Казахстана были хорошо известны образы на кости, в технике плавления и литья меди и бронзы. Такой техникой выполнены, к примеру, две большие бронзовые серьги из кургана Мыншункур, покрытые листовым золотом, на внутреннем ободе одной из которых припаяны две литые золотые фигурки лошадей. Курган Иссык располагается в западной половине могильника. Его диаметр 60 метров, высота — 6 метров. Внутри кургана находятся две погребальные камеры: центральная и боковая. Центральная неоднократно подвергалась разграблению. Боковая могила оказалась непотревоженной, захоронение и погребённый инвентарь сохранились полностью. Погребальная камера была сооружена из обработанных еловых брёвен. Могильник состоит из 45 больших царских курганов диаметром от 30 до 90 и высотой от 4 до 15 метров. Общая площадь некрополя — 3 км².
Объяснение: