По приведенной схеме реакции определите окислитель и восстановитель, составить электронный баланс, уравнять химическую реакцию, указать процессы окисления и восстановления
1. FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O.
2. H2S + KMnO4 + H2SO4 → S + MnSO4 + K2SO4 + H2O.
3.Ca3P2 + KMnO4 + H2SO4 → CaSO4 + H3PO4 + MnSO4 + K2SO4 + H2O.
ответ: ответ ниже. "⇒" и "=" заменить на стандартную "стрелочку" в химии.
Объяснение:
159) a)N( Степень окисления была -3, так как азот связан с тремя водородами, степень окисления которых равна +1) ⇒ N (степень окисления +2, так как связан с кислородом, степень окисления которого равна -2) ; Было -3, а стало +2, значит, N отдал 5 электрона.
б) O ( в 0 степени окисления, так как не связан больше ни с каким элементом) ⇒ O ( - 2 степень окисления, так как связан с двумя водородами, чья степень окисления равна +2) ; Было 0, а стало -2, значит, O получил 2 электрона.
Там 5 электронов, а здесь 2 электрона. Приводим к наименьшему общему кратному, домножая первую часть уравнения на 2, а вторую - на 5. Получаем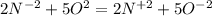 (К окислителю 2, к восстановителю 5) . В молекулярной форме это будет : 4NH3+5O2 ⇒ 4NO2 + 6H2O.
(К окислителю 2, к восстановителю 5) . В молекулярной форме это будет : 4NH3+5O2 ⇒ 4NO2 + 6H2O.
В 161 всё аналогично. Сразу перейду к коэффициентам
Инструкция по балансировке химических уравнений:
Введите уравнение химической реакции и нажмите "Уравнять". ответ на этот вопрос появится ниже
Всегда используйте верхний регистр для первого символа в названии химического элемента и нижнем регистре для второго символа. Например: Fe, Au, Co, C, O, N, F. Сравните: Co - кобальт и CO - угарный газ
Для уравнивания полуреакции окислительно-восстановительного процесса используйте {-} или е
Для обозначения зарядов ионов используйте фигурные скобки: {+3} или {3+} или {3}. Пример: Fe {3 +} +. I {-} = Fe {2 +} + I2
В случае сложных соединений с повторяющимися группами, замените неизменные части в формуле реагентов.
Например, уравнение C6H5C2H5 + O2 = C6H5OH + CO2 + H2O не будет сбалансированно,
но если C6H5 заменить на X, то все получится PhC2H5 + O2 = PhOH + CO2 + H2O
Примеры полных уравнений химического баланса:
Fe + Cl2 = FeCl3
KMnO4 + HCl = KCl + MnCl2 + H2O + Cl2
K4Fe(CN)6 + H2SO4 + H2O = K2SO4 + FeSO4 + (NH4)2SO4 + CO
C6H5COOH + O2 = CO2 + H2O
K4Fe(CN)6 + KMnO4 + H2SO4 = KHSO4 + Fe2(SO4)3 + MnSO4 + HNO3 + CO2 + H2O
Cr2O7{-2} + H{+} + {-} = Cr{+3} + H2O
S{-2} + I2 = I{-} + S
PhCH3 + KMnO4 + H2SO4 = PhCOOH + K2SO4 + MnSO4 + H2O
CuSO4*5H2O = CuSO4 + H2O
calcium hydroxide + carbon dioxide = calcium carbonate + water
sulfur + ozone = sulfur dioxide
Примеры химических уравнений реагентов (полное уравнение будет предложено):
H2SO4 + K4Fe(CN)6 + KMnO4
Ca(OH)2 + H3PO4
Na2S2O3 + I2
C8H18 + O2
hydrogen + oxygen
propane + oxygen