Процесс ОВР представлен уравнением :Р+Н2SO4 —>H3PO4+So2+H2O Определите степени окисления
Подчеркните элементы,изменившие свою степенью окисления в ходе реакции
Запишите процессы отдачи и принятия электронов методом электронного баланса
Составьте сбалансированное уравнение реакции
Запишите вещество, выполняющее роль окислителя
Запишите вещество, выполняющее роль восстановителя
Відповідь:
Выберите сколько вам нужно =)
Пояснення:
1. Хлорид натрия : для получения гидроксида натрия NaOH , хлора Cl₂ , пищевой соды NaHCO₃ .
2. Фосфат кальция Ca₃(PO₄)₂ — для получения фосфора P, фосфорной кислоты H₃PO₄, фосфорных удобрений.
3. Сульфиды служат сырьём для получения металлов (свинца Pb , цинка Zn , олова Sn ) и серной кислоты H₂SO₄ .
4. Карбонаты натрия (сода) Na₂CO₃ и калия (поташ) K₂CO₃ являются сырьём в производстве стекла и моющих веществ.
5. Карбонат кальция CaCO₃ служит сырьём в производстве негашёной извести CaO , a также в металлургии при выплавке чугуна и стали для выведения примесей в шлак.
1)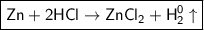 - молекулярное уравнение.
- молекулярное уравнение.
2)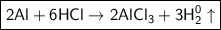 - молекулярное уравнение.
- молекулярное уравнение.
3)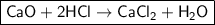 - молекулярное уравнение.
- молекулярное уравнение.
4)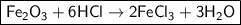 - молекулярное уравнение.
- молекулярное уравнение.
5) - молекулярное уравнение.
- молекулярное уравнение.
6)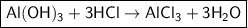 - молекулярное уравнение.
- молекулярное уравнение.
7) - молекулярное уравнение.
- молекулярное уравнение.